-
随着社会的快速发展,塑料制品被广泛应用于人们的工作与日常生活. 据研究,2015年全球塑料产量达到3.0×108 t[1]中国作为世界最大的塑料消费国之一,每年消耗塑料可达8000万t,然而其中只有30%被回收利用[2]. 大部分不可回收的塑料会通过焚烧或者丢弃的途径进入到环境中[3],而塑料难以被降解的特性会使其造成严重的环境污染[4]. 微塑料是由块状塑料在环境中破碎而来,通常是指直径小于5 mm塑料纤维、颗粒或者薄膜[5]. Su等的研究表明,太湖中微塑料丰度达0.01×106—6.8×106个·km−2[6]. 微塑料的漂浮性、耐腐蚀性、吸附性[7]使其不管是悬浮在海水中还是沉淀在沉积物中,都比普通塑料碎片要更加有害. 如在海洋中,微塑料会吸附有机污染物(如多氯联苯、壬基苯酚等)或无机污染物(汞、铅和锌等),这使其除了自身携带的有毒添加剂外,又负载了环境中的有毒污染物,导致微塑料整体毒性大大增加[8]. 一旦微塑料被生物误食或携带,就会将污染物通过食物链逐级传递,从而在生物体内富集,最终危害人类健康[9]. Evangeliou等的研究表明,大量累积的微塑料可能会加速北极冰雪圈的升温和融化[10]. 因此,需要有效的措施来减轻微塑料对水体环境的危害.
环境中常见的微塑料处理方法有物理法、生物降解法、化学法等[11]. 物理法主要有吸附、混凝、絮凝等[12-13]. 化学法包括化学吸附,光催化降解等[14-15]. 而生物降解法是通过生物分解这一过程以减少环境中微塑料含量[16]. 但是这些方法也存在一些局限性,如物理混凝与微塑料缺少表面相互作用而会导致其去除率较低(不到10%)[17]. 光催化对微塑料的降解并不完全[18]. 而生物降解通常需要较长的时间[19]. 因此在综合考虑成本和技术难度的情况下,吸附法是较为有潜力的一种微塑料去除方式.
生物炭是一种水环境中常用的吸附剂,它是由有机物在缺氧环境下热解而成[20-21]. 生物炭具有高表面积和微孔性,可以将污染物从水中吸附到自身上[22-23]. 生物炭的制备材料来源广泛,不同原料制成的生物炭在pH、灰分、比表面积、孔径等性质上均可能存在巨大的差异[24-25],从而影响生物炭的吸附性能. 此外,环境pH、吸附时间、初始污染物浓度等外部因素也会影响生物炭的吸附能力[26-27]. 然而有关不同种类生物炭对于微塑料吸附性能以及生物炭中检测微塑料的技术手段也在研究阶段.
本研究旨在探究不同原料制备的生物炭对微塑料吸附的性能差异,并尝试探索一种新的微塑料定量检测方法,以此为水环境中的微塑料污染修复提供新的思路和依据. 本研究采用污泥炭,玉米秸秆炭,梧桐皮炭的3种生物炭对比分析不同吸附时间,不同Cl−浓度干扰,不同pH情况下生物炭对微塑料PET(聚对苯二甲酸乙二醇酯)的吸附情况,采用拉曼光谱、衰减全反射红外光谱(ATR-IR)、扫描电镜(SEM)、热重分析等技术手段创新性验证生物炭对微塑料的吸附效果.
-
PET:聚对苯二甲酸乙二醇酯(Polyethylene terephthalate, (COC6H4COOCH2CH2O)n),熔点250—255 °C. PET是乳白色或浅黄色高度结晶性的聚合物,表面平滑光亮. PET耐磨擦、抗疲劳性和稳定性好,具有热塑性塑料中最大的韧性. PET受温度影响小,耐弱酸但不耐热水浸泡,不耐碱. 本次实验采用PET购买于澳港塑化公司,粒径为6.5 μm以下.
生物质炭的原料来源:污泥来自浙江永康污泥厂;秸秆来自淮安市玉米农田;梧桐皮来自南京理工大学校园自然凋零的梧桐皮. 试验所用试剂:氢氧化钠(NaOH, Aladdin)、氯化钠(NaCl, Aladdin)、浓盐酸(HCl, 南京理工大学药品库).
-
将污泥,秸秆,梧桐皮进行干燥粉碎,分别取0.15—0.25 mm的粉碎材料在马弗炉中以10 ℃·min−1升温速率在650 ℃热裂解3 h,然后进行自然冷却降温. 之后将生物炭过筛,取150 μm以上生物炭以备用. 在试验前,所用生物炭置于去离子水中并震荡20 min进行洗涤,然后再次取150 μm以上颗粒,在65 ℃条件下烘干72 h,以此去除生物炭中的杂质,防止其对实验干扰,此步骤重复3次.
-
采用ASAP 3020型比表面积孔径分析仪对三种生物炭进行孔隙分析. 采用Nicolet IS5型衰减全反射红外光谱(ATR-IR)对生物炭样品以500 cm−1至3500 cm−1的范围内用步长0.05的反射模式对信号进行3次采集,以此测定生物炭和微塑料的表面官能团,结果由OMNIC 8.2软件进行分析. 采用Aramis拉曼光谱仪采集微塑料的拉曼特征光谱,通过将微塑料的拉曼谱图与生物炭材料图谱进行比对,以确定生物炭上的微塑料的存在. 采用JSM-IT500HR型扫描电子显微镜(工作电压设为5 kV)对样品的表面形貌进行观察分析. 采用TGA/SDTA851E型热失重分析仪在氮气氛围下对吸附前后样品进行热重分析实验. 所有数据均采用Origin Lab 2017进行绘图制作.
-
在反应体系中,微塑料随时间变化会漂浮在液体表面或与生物炭一同沉降在液体底部,因此对吸附沉淀物后的生物炭和微塑料进行分离是一个难题,本研究参照现有方法[28-30],采用湿筛法和热重分析法相结合的方式进行定量分析. 湿筛法源自于分离土壤不同粒径的颗粒,以不加张力的单层土工布及其有关产品试样作为筛网,在规定的振动频率和振幅下,对试样以及颗粒级配材料(通常为砂土)进行喷水,使颗粒级配材料通过试样. 以通过的颗粒材料的特定粒径表示试样的有效孔径[31]. 在本实验中,生物炭和微塑料粒径存在明显差距,故采用湿筛法进行分离。预实验研究表明,在过滤过程中筛网上无明显微塑料挂网现象。主要实验步骤为将筛网置于玻璃收集器上,然后将反应后的溶液剧烈震荡20 s后过150 μm筛网,并进行喷水冲滤,分别收集筛网上固体与过滤下来的液体,收集液体前需将容器称重,然后将收集到的液体于80 ℃烘箱中烘干至恒定重量,测量收集液体前与烘干后重量变化确定过滤液中的微塑料重量.
式中,W1:生物炭吸附的微塑料重量g;W2:实验中微塑料的投加量g;W3:固体过滤物烘干后的总质量g;Q1:固体过滤物热重分析烧失量占比%;Q2:热重测试区间生物炭烧失量占比%;q:微塑料自身热重占比(本研究为88.99%).
-
称取3种生物炭各0.1 g分别加入20 mL浓度为0.5 g·L−1的PET溶液于50 mL离心管中. 将离心管置于摇床中,以25 ℃恒温下180 r·min−1震荡1、2、3、6、8、24 h. 试验结束后利用湿筛法分别收集固体与液体,每组实验设置3个重复. 采用Lagergren准一级动力学模型、准二级动力学模型对动力学吸附结果进行拟合[32].
-
取20 mL不同pH背景(pH=3、7、11)的PET溶液于50 mL离心管中,分别加入0.1 g生物炭,将离心管放在摇床中,以25 ℃和180 r·min−1的条件下恒温震荡6 h. 试验结束后利用湿筛法分别收集固体与液体,每组实验设置3个重复.
-
取20 mL不同NaCl背景浓度(0、0.05、0.1 g·L−1)的PET溶液于50 mL离心管中,分别加入0.1 g的3种生物炭,将离心管放在摇床中以25 ℃和180 r·min−1的条件恒温震荡6 h. 试验结束后利用湿筛法分别收集固体与液体,每组实验设置3个重复.
-
PET的红外光谱如图1A所示,在599、832、1246、1424、2021、2154 cm−1等处有较强的特征峰,可分别归于(C—H)的特征峰和(—CH2)的特征峰. PET的拉曼光谱(图1B)基线不水平,谱图呈现为弧形. 其中在637、701、849、965、1177、1425、2907 cm−1等处有明显的PET物质特征峰. PET的红外和拉曼谱图与后面3种生物炭的谱图相比有明显差异,因此这些PET的特征峰可以作为判断PET是否存在的依据.
-
PET的热重谱图如图1C所示. PET样品分解分为两个区间,252—375 ℃为第一个区间,PET在该区段分解率为64.29%,在306 ℃分解速率达到最大;383—517 ℃为第二个区间,PET在该区间段分解率为24.70%,在453 ℃分解速率达到最大. 520 ℃之后PET重量基本保持不变,残留可认为PET已经完全转化为残余物,因此这两个区间可以作为PET热解过程中总量测定区间(总热解比重为88.99%).
-
生物炭的孔隙结构特征如下表1所示. 从表中可以看出,3种生物炭平均孔径和总孔隙体积大小顺序为:污泥炭>梧桐皮炭>秸秆炭,其中梧桐皮炭和污泥炭的平均孔径和总孔隙体积相近. 3种生物炭比表面积大小顺序为:梧桐皮炭>污泥炭>秸秆炭.
-
图2分别为污泥炭、秸秆炭、梧桐皮炭的PET吸附动力学曲线. 随着吸附时间的增加,3种生物炭的吸附速率均呈现出先快后慢,最后趋于平衡的趋势. 污泥炭和秸秆炭的平衡时间约为6 h,梧桐皮炭的平衡时间约为4 h. 不同生物炭的吸附量呈现为梧桐皮炭>污泥炭>秸秆炭. 为研究不同生物炭对PET吸附动力学特性,采用Lagergren准一级动力学模型、准二级动力学模型分别对实验结果进行拟合,得到动力学参数如下表2所示,所有生物炭处理中准一级拟合曲线中的R2高于准二级方程拟合曲线的R2. 因此准一级方程能更好的描述生物炭对微塑料的吸附过程,证明3种生物炭对于微塑料的吸附以物理吸附为主.
生物炭吸附微塑料的吸附性实验证实,3种生物炭都对纳米级微塑料有很好的吸附能力. 不同类型生物炭的吸附动力学结果表明,污泥炭、秸秆炭、梧桐皮炭对微塑料的吸附分别在6 h、6 h、4 h达到吸附平衡. 在开始阶段,生物炭吸附速率均为梧桐皮炭>污泥炭=秸秆炭,这种现象主要是因为这一阶段的吸附主要以生物炭表面物理吸附为主(表2),梧桐皮炭的比表面积优于污泥炭,孔隙结构优于秸秆炭,这就使得其在前期吸附速率上具有明显优势. 吸附平衡时,污泥炭和梧桐皮炭的吸附量较为相近,二者远大于秸秆炭的吸附量,而相关性分析结果表明,生物炭对PET的吸附量与其比表面积(R2=0.98)和平均孔径(R2=0.67)有很高的相关性. 梧桐皮炭和污泥炭的总孔隙体积相近,但是污泥炭的平均孔径明显优于其他两种生物炭,而梧桐皮炭的比表面积远高于其他两种生物炭,这是导致这两种生物炭的吸附量大致相同的主要原因. 此外,梧桐皮炭虽然与污泥炭的吸附量相近,但是其吸附速率要高于污泥炭,因此证实比表面积是影响生物炭吸附微塑料速率的最主要的原因. 秸秆炭的比表面积、平均孔径和总孔隙体积远低于另外两种生物炭,因此其吸附效果最差.
-
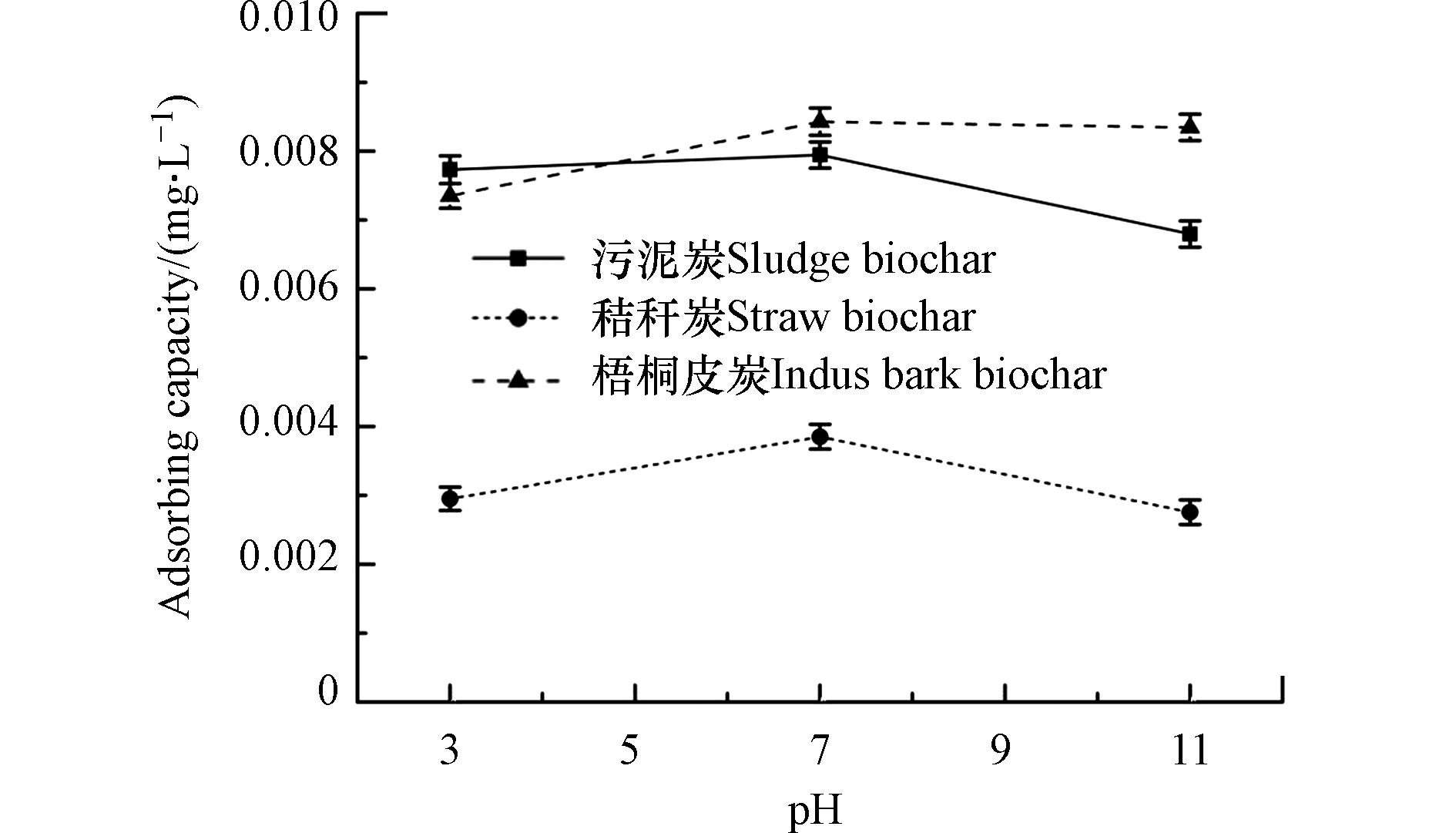
生物炭在不同pH的溶液环境下对微塑料的吸附量如下图3所示,溶液的pH环境不同会影响生物炭对微塑料吸附. 研究结果表明当pH3—7时,秸秆炭对微塑料的吸附量随pH的升高而升高(30.51%),梧桐皮炭随pH的升高而升高(14.70%),污泥炭无明显变化(2.71%). 在pH7—11时,秸秆炭对微塑料的吸附量呈现出下降的趋势(28.31%),污泥炭下降了14.36%,梧桐皮炭无明显变化. 3种不同材料的生物炭吸附效果为梧桐皮炭>污泥炭>秸秆炭. 在pH>7时,梧桐皮炭对微塑料的吸附量随着pH的升高而未发生明显变化,而污泥炭与秸秆炭吸附量下降较为明显. 这可能是由于在酸性环境下(pH=3—7),溶液中存在大量的H+,生物炭表面被质子化,并释放出大量阳离子,从而对阴离子产生静电吸引,而微塑料表面带有负电荷[33-34],这使得生物炭对微塑料的吸附能力增强. 在pH≥7时,由于随着pH的增大,生物炭表面阳离子被沉淀降低(如Ca(OH)2),因此导致生物炭逐渐带有负电荷,而生物炭与微塑料间的静电斥力作用使得生物炭对微塑料的吸附量下降. 因此,在一定在范围中,pH的增大不利于生物炭对微塑料的吸附.
-
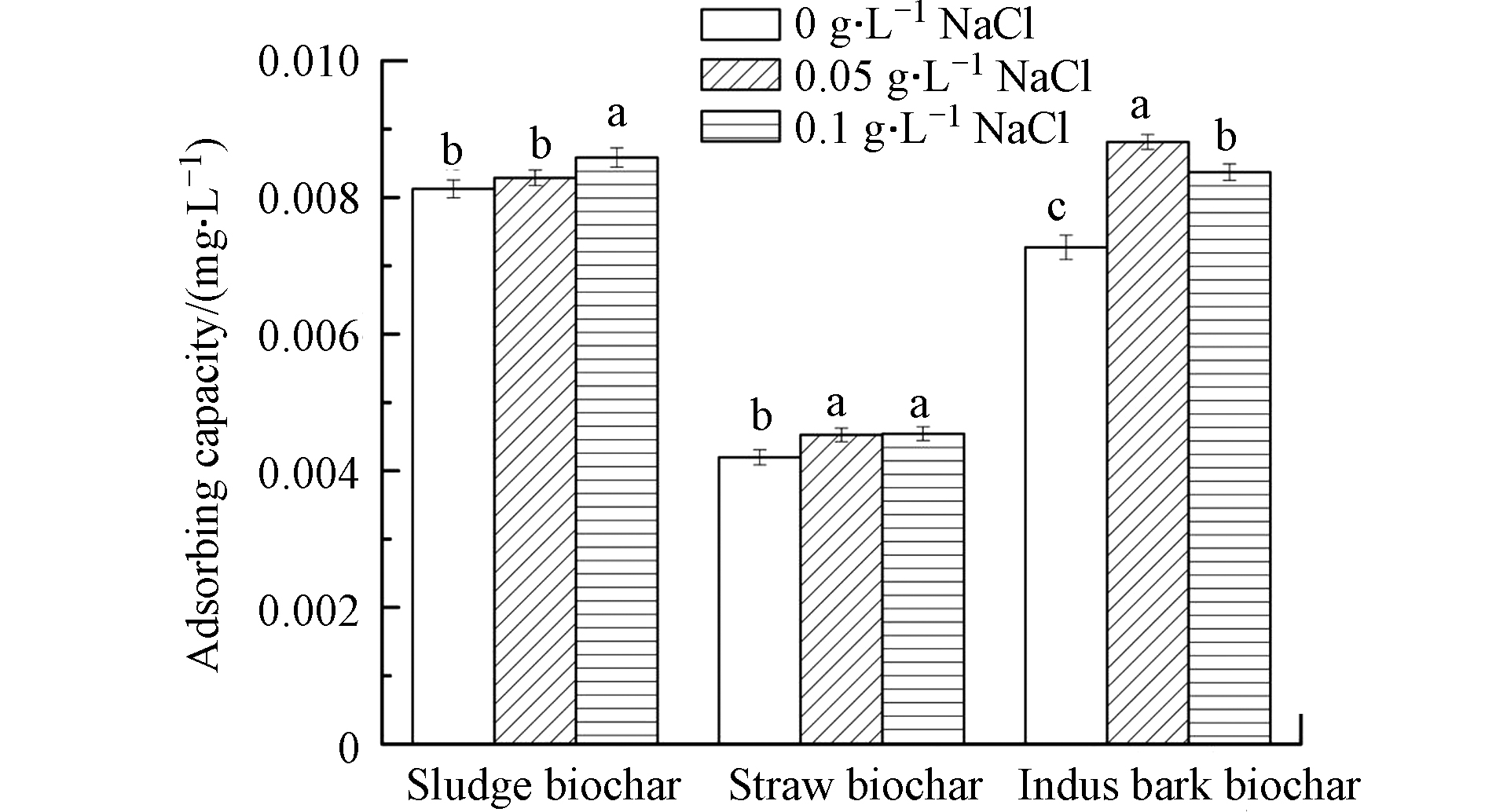
不同Cl−浓度的溶液环境下对微塑料的吸附量如下图4所示. 结果表明Cl−浓度对生物炭吸附微塑料的影响较小. 随着Cl−浓度的升高,3种生物炭吸附微塑料的量均有所提高,秸秆炭和梧桐皮炭均在0.05 g·L−1的Cl−浓度下吸附效果增大最明显. 污泥炭呈现随Cl−浓度的升高先增加后降低的趋势. 不同生物炭对溶液中微塑料的去除率随Cl−浓度变化与生物炭材料本身密切相关. 在低浓度至中浓度(0—0.05 g·L−1)时,3种炭材料对微塑料的吸附量均有所上升,其中梧桐皮炭吸附量增加最明显. 有研究表明,微塑料和生物炭对Cl−有很强的吸附性[35],因此二者在共同吸附少量Cl−的情况下有助于两种材料之间的吸引力. 而当中浓度到高浓度时(0.05—0.1 g·L−1),污泥炭吸附量略微上升,秸秆炭吸附量基本不变,梧桐皮炭吸附量略微下降. 这一现象可能是因为Cl−浓度的升高导致其侵占两种材料的吸附点位,从而阻碍了两种材料之间的吸引力. 此外,由于NaCl的浓度升高导致两种材料的悬浮界面差异增加,因此导致相互接触减少,这也可能导致高浓度下梧桐生物炭对微塑料吸附能力降低. 而环境中淡水和海水的Cl−浓度通常为200—19000 mg·L−1,因此生物炭完全可以在这一范围对微塑料进行吸附去除.
-
吸附微塑料前后生物炭的红外光谱图如图5所示。图5吸附后的红外光谱图从下至上为吸附1、2、6、8、24 h,显示出不同程度的锯齿状峰形,根据图1A中微塑料红外的特征峰,吸附后在599 、1424、2021 (污泥炭)、832 、1246 、2153 (秸秆炭)、599、2021 cm−1(梧桐皮炭)的位置均出现了明显的PET特征峰,说明3种生物炭材料上均有明显的微塑料吸附存在.
-
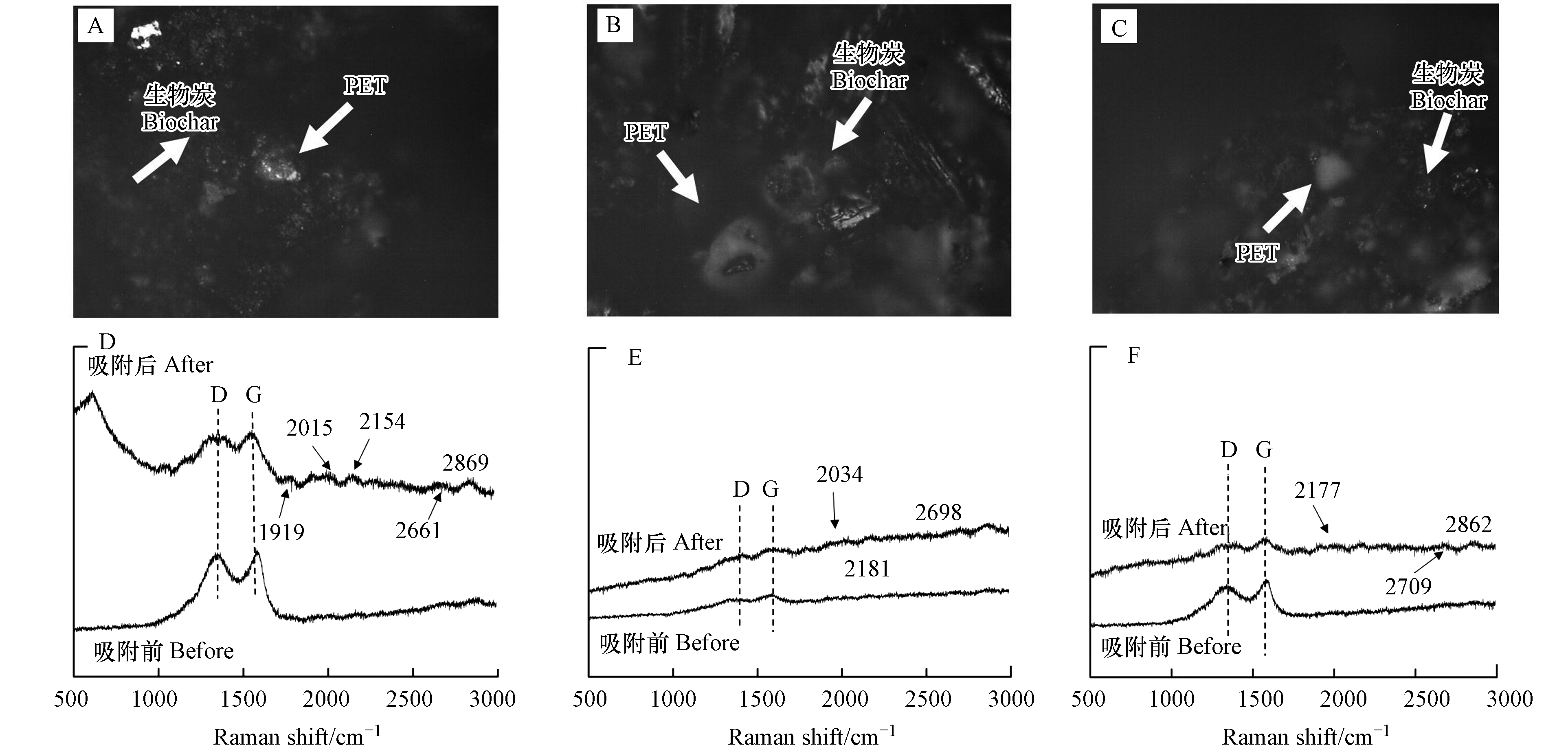
吸附后3种类型生物炭的拉曼光谱如图6所示. 3种生物炭拉曼图谱在1300 cm−1和1580 cm−1附近均只有2个特征峰,这两个峰分别对应D-峰和G-峰,表示材料的石墨化程度,是C原子晶体的特征峰. 此外,吸附后的生物炭拉曼形貌如图6A、B、C,在生物炭上有明显的白色颗粒物存在,而拉曼谱图如图6D、E、F所示. 对于污泥炭的吸附后拉曼光谱图可以明显看到637 cm−1处出现峰值,在2901 cm−1处也略微出现峰值,说明拉曼光谱在污泥炭吸附后的样品中检测出了微塑料. 秸秆炭和梧桐皮炭的拉曼光谱在500—700 cm−1明显上升,并且在2177、2181、2871 cm−1处有PET的特征峰存在,因此证实两种生物炭上均存在PET微塑料.
-
扫描电镜下可以观察到PET的形貌多为球状颗粒,表面或存在凹陷,粒径多在1 μm以下(图7). 吸附后生物炭的扫描电镜图中,3种生物炭表面均有明显的PET颗粒存在,并且分布不均匀.
-
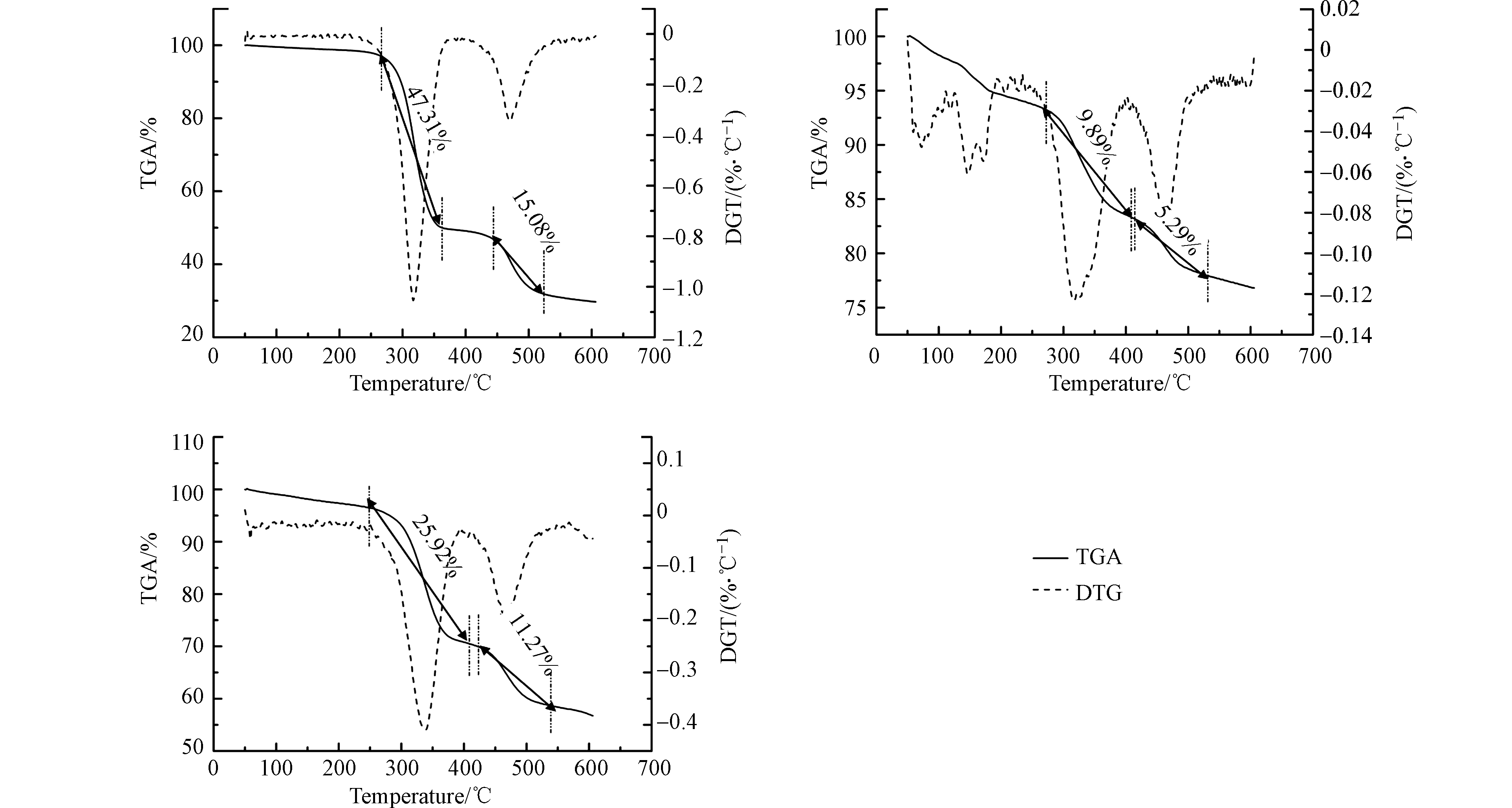
吸附微塑料过后3种生物炭热重分析图如图8所示. 3种生物炭均出现了PET样品分解速率增大的两个特征区间,污泥炭样品的烧失量为62.39%,秸秆炭样品为15.18%,梧桐皮炭样品为37.19%,3种炭样品的微塑料含量梧桐皮炭>污泥炭>秸秆炭,这与吸附动力学的结果一致.
与微塑料标准样品相比吸附后生物炭的热重区间略微向右偏移,这有可能是因为生物炭自身微量可分解物质产生导致. 但是PET分解速率增大的特殊区间仍然可以用来鉴别微塑料. 其中污泥炭和梧桐皮炭在热重时炭材料本身分解量小,秸秆炭在热重时分解量大,但是对于实验比较生物炭的吸附效果结论没有影响.
-
对比分析吸附后生物炭的热重分析法和热重-湿筛联合分析法的结果发现(表3),与热重分析法相比,在热重-湿筛联合分析法计算得到的三种生物炭样品的微塑料含量明显少于前者,且误差更小. 这一结果证实,热重-湿筛联合分析法可以将透过筛网之下的炭和微塑料带入计算,从而避免由于只考虑筛网之上或筛网之下样品的误差,因此能更加准确的计算出吸附后生物炭中的微塑料含量. 此外,热重-湿筛联合分析法得到3种炭样品的微塑料含量梧桐皮炭>污泥炭>秸秆炭,这与热重分析法的结果趋势一致.
综合红外光谱,拉曼光谱,扫描电镜的检测结果. 在红外光谱下可以看到部分PET的特征峰,但是与3种生物炭材料比对发现PET红外峰与生物炭材料的峰有所重叠,这使得在PET含量较小时难以直接从红外光谱中进行直接鉴别. 红外光谱检测可以看到,3种生物炭材料均出现锯齿状峰形,污泥炭和秸秆炭在约2021 cm−1处有弱峰,这是因双键的伸缩振动所致,秸秆炭在约832 cm−1处存在C—H键的摇摆振动. 污泥炭炭在约 599 cm−1处存在(—OH)的吸收峰. 这表明生物炭表面以羟基、不饱和键的形式参与微塑料的吸附[34]. 在拉曼光谱下PET的拉曼光谱基线不水平,未矫正基线时谱图呈现为弧形. 在637 cm−1、701cm−1处的吸收峰和在2907 cm−1处的吸收峰并未与炭材料重叠,在吸附后样品中成功测出. 由于本实验设计添加微塑料含量较低,在红外光谱和拉曼光谱观察到吸附实验过后部分生物炭上微塑料的特征峰较弱,只可以进行定性分析,不足以进行半定量分析. 热重分析法可以明显定量检测出生物炭上的微塑料,但是其受到实验过程中炭和微塑料的操作损耗影响严重,因此也不能完全独立用于生物炭吸附微塑料的研究. 因此,相比直接使用热重分析法进行测定,本研究采用的湿筛-热重联用分析法主要以晒网所过滤的固体进行分析,这能够将在实验过程中破碎或微小的炭粒计算进去,避免了直接分析带来的误差. 此外,根据相关性分析的结果,本研究进一步证实影响生物炭吸微塑料的自身主要因素为平均孔径(R2=0.67)、比表面积(R2=0.98),而pH(R2=0.98)和Cl−(R2=0.69)干扰因素分别对梧桐生物炭和污泥生物炭吸附微塑料有很好的正相关性.
-
(1)不同生物炭对溶液中微塑料吸附性能不同,本次实验选取了污泥炭,秸秆炭,梧桐皮炭. 通过吸附动力学实验,不同pH和Cl−浓度对生物炭吸附微塑料性能的影响实验发现,3种生物炭对微塑料的吸附效果在3种情况下综合为梧桐皮炭=污泥炭>秸秆炭. 其中秸秆炭在实验中易碎,吸附效果最差,难以应用于实际,不适合用于吸附微塑料.
(2)对不同生物炭对溶液中微塑料吸附性能研究中,发现3种不同生物炭对水溶液中微塑料的吸附速率呈现先快后慢,最后趋于平衡的趋势,梧桐皮炭吸附效果最好. 吸附动力学分析结果表明,3种生物炭对PET的吸附主要以物理吸附为主. 不同pH对生物炭吸附微塑料性能的影响,不同Cl−浓度对生物炭吸附微塑料性能的影响的实验表明外界因素对生物炭吸附微塑料有一定影响,影响程度与生物炭本身的性质有关.
(3)本研究采用的湿筛-热重联用分析法成功定量检测出生物炭上的微塑料.相比直接使用热重分析法进行测定,湿筛-热重联用分析法主要以晒网所过滤的固体进行分析,这能够将在实验过程中破碎或微小的炭粒计算进去,避免了直接分析带来的误差.
不同类型生物炭对水体中微塑料的吸附性能
Sorption properties of microplastics in water by different types of biochar
-
摘要: 微塑料自生的毒性和富集作用会极大地危害生物健康. 不同原材料,生物炭结构组成不同,吸附特性也不一样. 探究不同类型生物炭对微塑料的吸附性能及吸附机理,有助于为生物炭吸附去除水体中微塑料的材料选择提供理论依据.本研究使用3种有机废弃物制备成的生物炭(污泥炭,秸秆炭,梧桐皮炭)对微塑料PET(6.5 μm)进行吸附试验,通过比表面积和孔径分析、衰减全反射红外光谱、拉曼光谱、湿筛法-热重联用分析法多种技术手段分别定性和定量研究不同反应时间、不同Cl−浓度和溶液初始pH对生物炭吸附微塑料的影响. 研究结果证实生物炭上存在明显的微塑料,吸附动力学研究表明准一级方程能更好的描述生物炭对微塑料的吸附过程,证明3种生物炭对于微塑料的吸附以物理吸附为主,吸附分别在5—10 h时达到平衡. 3种生物炭吸附能力大小为梧桐皮炭=污泥炭>秸秆炭. 生物炭对微塑料的吸附量均随着pH的升高先升高(pH3—7)后降低(pH7—11). 此外,Cl−浓度对生物炭吸附微塑料影响较小. 随着微塑料浓度提升,3种生物炭吸附微塑料的量均有提高.生物炭的平均孔径和比表面积是影响其吸附微塑料的主要原因. 另外,本研究创新的湿筛-热重联用分析法由于减少了实验过程中破碎生物炭的影响,比热重分析法更加准确定量检测微塑料.Abstract: The toxicity and enrichment of microplastics themselves will greatly harm biological health. Different raw materials lead to different structure and composition of biochar, so its adsorption characteristics are different. To explore the adsorption properties and mechanism of different types of biochar on microplastics, it can provide theoretical basis for the selection of materials for the adsorption and removal of microplastics from water by biochar. In this study, biochar prepared from three kinds of organic wastes (Sludge biochar, Straw biochar, and Sycamore bark biochar) was used to adsorb PET (6.5 μm) of microplastics. The effects of different reaction time, different Cl− concentration and solution initial pH on biochar adsorption of microplastic were qualitatively and quantitatively studied by using specific surface area and pore size analysis, attenuated total reflection infrared spectroscopy, Raman spectroscopy and wet sieve-thermogravimetric analysis. The results confirmed the presence of significant microplastics on biochar. The adsorption kinetics study shows that the pseudo first order equation can better describe the adsorption process of micro plastics on biochar, it was proved that the adsorption of the three kinds of biochar on microplastics was mainly physical adsorption, and the adsorption reached equilibrium at 5—10 h respectively. The adsorption capacity of the three biochar was as follows: Indus bark biochar=sludge biaochr and > straw bichar. The adsorption capacity of biochar on microplastics increased first pH(3—7) and then decreased with the increase of pH (7—11). Furthermore, Cl− concentration has little effect on biochar adsorption of microplastics. When the concentration of microplastics increased, the amount of microplastics adsorbed by the three kinds of biochar increased. The average pore size and specific surface area of biochar are the main factors affecting the adsorption of microplastics. In addition, the innovative wet sieve-thermogravimetric analysis method in this study is more accurate than thermogravimetric analysis in quantitative detection of microplastics because it reduces the impact of broken biochar in the experimental process.
-
Key words:
- biochar /
- microplastics /
- wet sieving /
- thermogravimetric analysis /
- physical adsorption
-

-
表 1 生物炭孔隙结构特征
Table 1. Pore structure characteristics of biochar
生物炭
Biochar比表面积/(m2·g−1)
BET平均孔径/nm
Average pore size总孔隙体积/(cm3·g−1)
Total pore volume污泥炭 21.660 3.189 0.056 秸秆炭 16.320 0.725 0.016 梧桐皮炭 176.350 1.800 0.051 表 2 不同生物炭吸附微塑料动力学参数
Table 2. Kinetic parameters of different biochar adsorption microplastics
准一级模型参数 生物炭Biochar qe /(mg·g−1) k1 /(min−1) R2 Parameter of quasi-first order model 污泥炭 0.008 0.553 0.832 秸秆炭 0.004 0.514 0.709 梧桐皮炭 0.008 0.727 0.845 准二级模型参数 生物炭Biochar qe /(mg·g−1) k2 /(mg·min)−1) R2 Quasi-second order model parameters 污泥炭 0.009 0.658 0.832 秸秆炭 0.004 0.386 0.679 梧桐皮炭 0.009 0.518 0.689 表 3 热重分析法和热重-湿筛联合分析法对比
Table 3. Comparison of thermogravimetric analysis and combined thermogravimetric and wet-screen analysis
方法
Method生物炭种类
Species of biochar吸附微塑料的重量/mg
Weight of the adsorbed microplastics热重分析法
Thermogravimetric analysis污泥炭 0.53±0.13 秸秆炭 0.38±0.09 梧桐皮炭 1.44±0.11 热重-湿筛联合分析法
Combined thermogravimetric and wet-screen analysis污泥炭 0.40±0.07 秸秆炭 0.31±0.06 梧桐皮炭 1.26±0.03 -
[1] CHEN X, YAN N. A brief overview of renewable plastics [J]. Materials Today Sustainability, 2020, 7/8: 100031. doi: 10.1016/j.mtsust.2019.100031 [2] WANG G, WANG J S, XUE Q G. Efficient utilization of waste plastics as raw material for metallic iron and syngas production by combining heat treatment pulverization and direct reduction [J]. Process Safety and Environmental Protection, 2020, 137: 49-57. doi: 10.1016/j.psep.2020.02.017 [3] CHEN Y D, CUI Z J, CUI X W, et al. Life cycle assessment of end-of-life treatments of waste plastics in China [J]. Resources, Conservation and Recycling, 2019, 146: 348-357. doi: 10.1016/j.resconrec.2019.03.011 [4] 江秀萍. 海洋微塑料的来源及其危害 [J]. 南方农机, 2019, 50(15): 276-277. JIANG X P. Source and harm of marine microplastics [J]. China Southern Agricultural Machinery, 2019, 50(15): 276-277(in Chinese).
[5] EGESSA R, NANKABIRWA A, OCAYA H, et al. Microplastic pollution in surface water of Lake Victoria [J]. Science of the Total Environment, 2020, 741: 140201. doi: 10.1016/j.scitotenv.2020.140201 [6] SU L, XUE Y G, LI L Y, et al. Microplastics in Taihu lake, China [J]. Environmental Pollution, 2016, 216: 711-719. doi: 10.1016/j.envpol.2016.06.036 [7] ROCHMAN C M, BROWNE M A, HALPERN B S, et al. Classify plastic waste as hazardous [J]. Nature, 2013, 494(7436): 169-171. doi: 10.1038/494169a [8] 赵淑江, 王海雁, 刘健. 微塑料污染对海洋环境的影响 [J]. 海洋科学, 2009, 33(3): 84-86. ZHAO S J, WANG H Y, LIU J. Influence of microplastics pollution on marine environment [J]. Marine Sciences, 2009, 33(3): 84-86(in Chinese).
[9] MOORE C J, MOORE S L, LEECASTER M K, et al. A comparison of plastic and plankton in the north Pacific central gyre [J]. Marine Pollution Bulletin, 2001, 42(12): 1297-1300. doi: 10.1016/S0025-326X(01)00114-X [10] EVANGELIOU N, GRYTHE H, KLIMONT Z, et al. Atmospheric transport is a major pathway of microplastics to remote regions [J]. Nature Communications, 2020, 11: 3381. doi: 10.1038/s41467-020-17201-9 [11] 刘江峡, 刘欢, 刘清泉, 等. 多层级孔材料及水体微塑料处理的研究进展 [J]. 合成材料老化与应用, 2020, 49(2): 103-108. LIU J X, LIU H, LIU Q Q, et al. Research progress of hierarchical porous materials and treatment of water micro-plastics pollution [J]. Synthetic Materials Aging and Application, 2020, 49(2): 103-108(in Chinese).
[12] 袁芳, 岳灵芝, 周俊, 等. 一种采用三维石墨烯吸附水中聚苯乙烯微塑料的方法: CN110559995A[P]. 2019-12-13. YUAN F, YUE L Z, ZHOU J, et al. Method for adsorbing polystyrene microplastics in water by adopting three-dimensional graphene: CN110559995A[P]. 2019-12-13(in Chinese).
[13] RAJALA K, GRÖNFORS O, HESAMPOUR M, et al. Removal of microplastics from secondary wastewater treatment plant effluent by coagulation/flocculation with iron, aluminum and polyamine-based chemicals [J]. Water Research, 2020, 183: 116045. doi: 10.1016/j.watres.2020.116045 [14] ARIZA-TARAZONA M C, VILLARREAL-CHIU J F, BARBIERI V, et al. New strategy for microplastic degradation: Green photocatalysis using a protein-based porous N-TiO2 semiconductor [J]. Ceramics International, 2019, 45(7): 9618-9624. doi: 10.1016/j.ceramint.2018.10.208 [15] 徐擎擎, 张哿, 邹亚丹, 等. 微塑料与有机污染物的相互作用研究进展 [J]. 生态毒理学报, 2018, 13(1): 40-49. XU Q Q, ZHANG G, ZOU Y D, et al. Interactions between microplastics and organic pollutants: Current status and knowledge gaps [J]. Asian Journal of Ecotoxicology, 2018, 13(1): 40-49(in Chinese).
[16] KARIM M E, SANJEE S A, MAHMUD S, et al. Microplastics pollution in Bangladesh: Current scenario and future research perspective [J]. Chemistry and Ecology, 2020, 36(1): 83-99. doi: 10.1080/02757540.2019.1688309 [17] LAPOINTE M, FARNER J M, HERNANDEZ L M, et al. Understanding and improving microplastic removal during water treatment: Impact of coagulation and flocculation [J]. Environmental Science & Technology, 2020, 54(14): 8719-8727. [18] ARIZA-TARAZONA M C, VILLARREAL-CHIU J F, HERNÁNDEZ-LÓPEZ J M, et al. Microplastic pollution reduction by a carbon and nitrogen-doped TiO2: Effect of pH and temperature in the photocatalytic degradation process [J]. Journal of Hazardous Materials, 2020, 395: 122632. doi: 10.1016/j.jhazmat.2020.122632 [19] ZHANG X L, CHEN J X, LI J. The removal of microplastics in the wastewater treatment process and their potential impact on anaerobic digestion due to pollutants association [J]. Chemosphere, 2020, 251: 126360. doi: 10.1016/j.chemosphere.2020.126360 [20] 孟莉蓉, 俞浩丹, 杨婷婷, 等. 2种生物炭对Pb、Cd污染土壤的修复效果 [J]. 江苏农业学报, 2018, 34(4): 835-841. MENG L R, YU H D, YANG T T, et al. Immobilization of two biochars to Pb, Cd in contaminated soils [J]. Jiangsu Journal of Agricultural Sciences, 2018, 34(4): 835-841(in Chinese).
[21] 顾博文, 曹心德, 赵玲, 等. 生物质内源矿物对热解过程及生物炭稳定性的影响 [J]. 农业环境科学学报, 2017, 36(3): 591-597. GU B W, CAO X D, ZHAO L, et al. Influence of inherent minerals on biomass pyrolysis and carbon stability in biochar [J]. Journal of Agro-Environment Science, 2017, 36(3): 591-597(in Chinese).
[22] YANG X B, YING G G, PENG P A, et al. Influence of biochars on plant uptake and dissipation of two pesticides in an agricultural soil [J]. Journal of Agricultural and Food Chemistry, 2010, 58(13): 7915-7921. doi: 10.1021/jf1011352 [23] YU X Y, YING G G, KOOKANA R S. Reduced plant uptake of pesticides with biochar additions to soil [J]. Chemosphere, 2009, 76(5): 665-671. doi: 10.1016/j.chemosphere.2009.04.001 [24] 彭启超, 刘小华, 罗培宇, 等. 不同原料生物炭对氮、磷、钾的吸附和解吸特性 [J]. 植物营养与肥料学报, 2019, 25(10): 1763-1772. PENG Q C, LIU X H, LUO P Y, et al. Adsorption and desorption characteristics of nitrogen, phosphorus and potassium by biochars from different raw materials [J]. Journal of Plant Nutrition and Fertilizers, 2019, 25(10): 1763-1772(in Chinese).
[25] 宋婷婷, 李洁, 张贵龙, 等. 不同原料生物炭对水体硝态氮的吸附性能研究[J]. 生态环境学报, 2018, 27(2): 330-340 SONG T T, LI J, ZHANG G L, et al. Study on the adsorption capacity of different raw materials biochar for nitrate nitrogen in water. Journal of Ecology and Environment, 2018, 27(2): 330-340.
[26] 孙耀胜, 么强, 刘竞依, 等. 生物炭材料在水体有机污染治理中的研究进展 [J]. 环境科学与技术, 2021, 44(1): 170-180. SUN Y S, YAO Q, LIU J Y, et al. Research progress of biochar materials in treatment of organic pollution in water [J]. Environmental Science & Technology, 2021, 44(1): 170-180(in Chinese).
[27] 刘凌言, 陈双荣, 宋雪燕, 等. 生物炭吸附水中磷酸盐的研究进展 [J]. 环境工程, 2020, 38(11): 91-97. LIU L Y, CHEN S R, SONG X Y, et al. Research progress in removal of phosphate from water by biochar [J]. Environmental Engineering, 2020, 38(11): 91-97(in Chinese).
[28] 王昆, 林坤德, 袁东星. 环境样品中微塑料的分析方法研究进展 [J]. 环境化学, 2017, 36(1): 27-36. WANG K, LIN K D, YUAN D X. Research progress on the analysis of microplastics in the environment [J]. Environmental Chemistry, 2017, 36(1): 27-36(in Chinese).
[29] SUN J, DAI X H, WANG Q L, et al. Microplastics in wastewater treatment plants: Detection, occurrence and removal [J]. Water Research, 2019, 152: 21-37. doi: 10.1016/j.watres.2018.12.050 [30] 王俊豪, 梁荣宁, 秦伟. 海洋微塑料检测技术研究进展 [J]. 海洋通报, 2019, 38(6): 601-612. WANG J H, LIANG R N, QIN W. Review of analytical methods for detecting microplastics in the ocean [J]. Marine Science Bulletin, 2019, 38(6): 601-612(in Chinese).
[31] 中华人民共和国国家质量监督检验检疫总局. 中华人民共和国推荐性国家标准: 土工布及其有关产品有效孔径的测定 湿筛法 GB/T 17634—1998[S]. 北京: 中国标准出版社, 1999. General Administration of Quality Supervision, Inspection and Quarantine of the People's Republic of China. National Standard (Recommended) of the People's Republic of China: Geotextiles and geotextile-related products-Determination of the characteristic opening size-Wet sieving method. GB/T 17634—1998[S]. Beijing: Standards Press of China, 1999(in Chinese).
[32] GONG H B, TAN Z X, ZHANG L M, et al. Preparation of biochar with high absorbability and its nutrient adsorption-desorption behaviour [J]. Science of the Total Environment, 2019, 694: 133728. doi: 10.1016/j.scitotenv.2019.133728 [33] 张国胜, 程红艳, 张海波, 等. 双孢菇菌糠生物炭吸附Pb2+机制及其环境应用潜力 [J]. 农业环境科学学报, 2021, 40(3): 659-667. ZHANG G S, CHENG H Y, ZHANG H B, et al. Adsorption mechanism of Pb2+ in water by biochar derived from spent Agaricus bisporus substrate and its environmental application potential [J]. Journal of Agro-Environment Science, 2021, 40(3): 659-667(in Chinese).
[34] LI X N, JIANG X, SONG Y, et al. Coexistence of polyethylene microplastics and biochar increases ammonium sorption in an aqueous solution [J]. Journal of Hazardous Materials, 2021, 405: 124260. doi: 10.1016/j.jhazmat.2020.124260 [35] 刘海朱, 王隽媛, 路思远, 等. 微塑料对有机污染物的吸附及微塑料-有机物复合污染的毒性研究进展 [J]. 环境生态学, 2020, 2(12): 89-94. LIU H Z, WANG J Y, LU S Y, et al. Research progress on adsorption of organic pollutants by microplastics and toxicity of microplastic-organic compound pollution [J]. Environmental Ecology, 2020, 2(12): 89-94(in Chinese).
-




 下载:
下载: