-
地球上存在许多天然光催化物质和人工合成光催化物质,光催化物质发生的光催化反应,内在机理在于高活性电子(e-)-空穴(h+)对的光激发。自由电子存在的能带称为导带,自由空穴存在的能带称为价带,电子-空穴对是在光的照射下,价带上的电子跃迁到导带上后,由导带上的电子和价带上的空穴组成的[1-3],而电子从价带跃迁到导带所需能量的最小值称为禁带宽度[4]。电子-空穴与光催化物质表面的电子受体或电子供体反应会生成的具有高活性的中间物质,即光生自由基,如单线态氧(1O2)、羟基自由基 (·OH)、超氧负离子(O2-·)等[5]。
光催化物质可应用于污染物的降解、自清洁材料的制备、生物疾病的治疗等多个方面[6],具有成本低、无二次污染等突出优点,得到人们的普遍认可,有关光催化的出版物数量呈线性逐年增加[7]。近年来,许多自然界中存在的天然物质具备的光催化特性陆续被发现,该类天然物质对驱动地球生物化学循环、地表污染物迁移转化产生着不可忽视的影响[8],然而目前大部分研究者的关注点仍在于如何制备新型高效人工复合型光催化物质,对天然光催化物质的综述文献极少。因此,本论文将总结自然环境中具备光催化性能的天然物质,介绍其光催化参数,解析其发生光催化的原理,阐述其环境效应与应用前景,并从效应研究和工程应用角度展望其今后的发展方向。
-
判断一种天然物质是否具备光催化特性及其光催化性能的优劣,需要对以下光催化相关参数进行表征:
(1)价带(valence band, VB)和导带(conduction band, CB):价带和导带的位置分别反映了空穴和电子的氧化还原电位的大小,只有当价带空穴的氧化还原电位较反应物更正时,光催化氧化反应才可能发生;反之,当导带电子的氧化还原电位较反应物更负时,光催化还原反应才可能发生[9]。紫外-可见积分球漫反射光谱可以方便获得光催化物质的带边位置,是研究光催化材料光学性质的重要表征手段。其主要原理是光催化物质吸收紫外-可见光波段的能量,其价带电子由价带顶跃迁至导带底,产生吸收,形成该物质的紫外-可见漫反射光谱。
(2)带隙(band gap):价带和导带之间的能量间隔称为带隙,也叫禁带宽度。禁带宽度决定了光催化物质的光响应范围,是影响光催化活性的一个重要因素[10]。过宽或过窄的禁带宽度均不利于光电子的产生、转移与转化。禁带宽度过大,产生的光生电子-空穴对虽然具有强氧化性,但数量少,光催化效率不高。禁带宽度过小,虽然能产生大量光生电子-空穴对,但其氧化能力太低,且电子更容易从激发态回到基态,光生电子-空穴的复合急剧增加,光催化效率同样会下降。只要光催化材料吸收的光能量大于禁带宽度,就有光催化活性。其测定同样可用紫外-可见积分球漫反射光谱,结合紫外-可见漫反射光谱与库贝尔卡-蒙克(Kubelka-Munk)方程可计算光催化物质的带隙。
(3)光电流密度(photocurrent density): 具有光化学特性的物体在光的照射下产生光电效应,发射出电子,电子在电场中定向移动形成电流,这种电流叫光电流(即光生载流子的定向运动形成光电流)。光电流密度是电荷流动的密度,即每单位截面面积的电流量,其大小反映了天然光催化物质光化学活性大小。光电流密度的测量是在三电极体系的化学工作站中进行的,一般将光催化物质负载在氧化铟锡工作电极上[11]。如果出现光照时电极电流密度显著提升,断开光源后电流瞬间减小至光照前状态的现象,且重复性好,说明该物质具有良好的光电催化活性。
(4)吸收波长(absorption wavelength):光催化物质的吸收波长是从紫外-可见分光光度法测得的吸收光谱获得。其基本原理是:光子作用于物质分子时,如果光子的能量与物质分子的电子能级满足特定能级差,光子将能量传递给物质分子,分子获得能量可发生电子能级的跃迁。在光吸收过程中基于分子中电子能级的跃迁而产生的光谱,称为紫外-可见吸收光谱。某物质的吸收曲线则反映的是该物质对不同波长单色光的吸收程度,其中波长为横坐标,吸光度为纵坐标。由于同一种吸光物质对不同波长的光吸收程度不同,吸光度最大处(即波峰处)对应的波长称为最大吸收波长。
(5)表面性质:光催化物质的表面性质对其光催化性能也有一定影响。固体光催化物质在形态上有意义的特征包括表面积、孔大小、孔体积的分布和密度等。这些表面特征的表征手段包括X-射线衍射、扫描电子显微镜、电子能谱、傅里叶变换红外光谱、漫反射光谱等[7, 12]。研究表明,比表面积小、孔隙率大、孔径分布宽的天然物质更有利于光的吸收[13-15]。
-
天然金属矿物中的锐钛矿(TiO2)、闪锌矿(ZnS)、赤铁矿(Fe2O3)、黑锡矿 (SnO)、辉钨矿 (SnS2)、铅黄(PbO)、硫镉矿(CdS)等多种氧化物和硫化物均具有光催化活性。表1列举了具有代表性天然光催化矿物的特征参数。自然界中大多数金属氧化物矿物半导体带隙能大于1.5 eV,产生光电子的最大波长范围是249—777 nm,主要吸收可见光,少部分吸收紫外光。大部分金属硫化物矿物半导体带隙能小于1.5 eV,产生光电子的最大波长范围大于921 nm,主要吸收红外光,少部分吸收可见光[9],参见图1。鲁安怀等[8, 16]在我国南方红壤、 西南喀斯特和西北戈壁等典型陆地生境中,发现直接暴露于太阳光下的土壤/岩石表面广泛发育有几十纳米到数百微米厚度的由铁锰氧化物组成的 “矿物膜”,首次提出“矿物膜”的概念,并证实了铁锰氧化物矿物膜可以驱动光电子生成与传递。他们利用电子束蒸发显微镀膜技术,制备显微电化学回路,光源开启时,“矿物膜”可以产生灵敏的光电流信号,且光电流随着时间的延长基本不变,呈现出优良的光稳定性特征,而地下岩石矿物则无光电流响应[17]。
-
天然色素来源于植物的根、茎、叶以及少部分动物和微生物体内,也是一类天然光催化物质。天然色素主要分三大类,即叶绿素、类胡萝卜素和藻胆素,根据分子结构的区别又可细分更多小类(表2)。
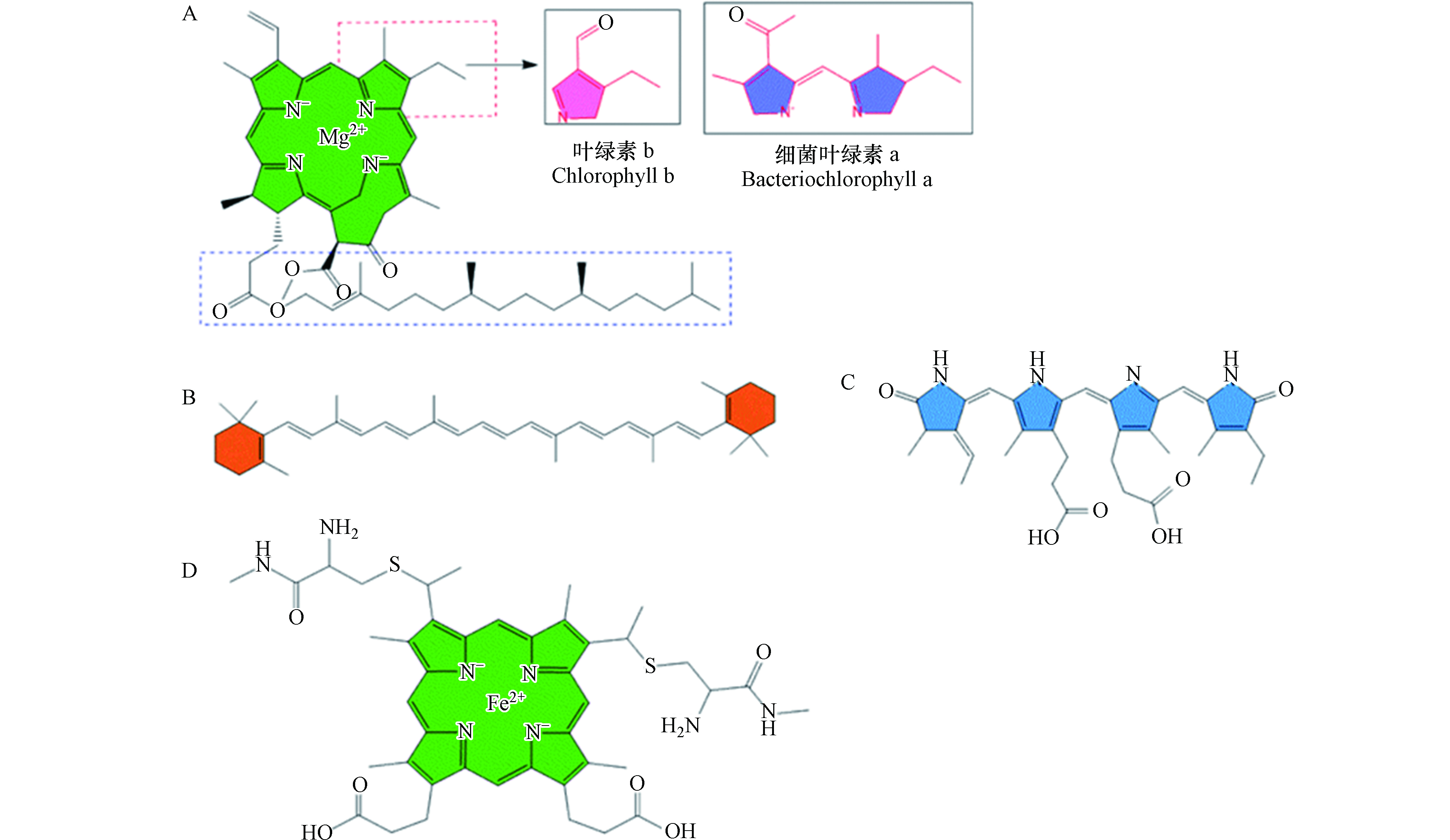
叶绿素是一类与光合作用密切相关的色素,其存在于大多数绿色植物体内,叶绿素分子的核心部分是一个特殊的卟啉环结构(图2A),其主要功能是收集光能,将能量转移到反应中心并驱动反应中心的电荷分离[22-24]。叶绿素除了常见的叶绿素a、b、c和 d,还包括叶绿素f以及细菌叶绿素。结构决定性质,叶绿素母环上不同的非对称基本骨架以及所连带的活性取代基团,决定了该类化合物在化学反应方面所表现出来的特定性质[25],如图2A红框或蓝框所示结构的差异,例如叶绿素c没有其它叶绿素共有的长脂肪烃侧链——叶绿醇(即图2A蓝框部分),导致了每种叶绿素具有不同的光吸收波长,这是区分它们的一大特性。叶绿素的光敏特性使其在有氧的条件下,可将光能量转移到分子氧的三重态基态从而产生自由基1O2 和·OH[26-28],其中1O2占主要部分, 1O2 和·OH都是活性氧物种(reactive oxygen species,ROS),具有较强的氧化性[5]。类胡萝卜素(图2B)和藻胆素(图2C)是对叶绿素捕获光能的补充,属于辅助色素,它们较长的共轭双键决定了其具有较宽的吸收光区,因此补充了叶绿素吸收较差的红绿光区,在吸收和传递能量方面发挥了重要作用[29-30]。类胡萝卜素是光合作用生物产生的亲脂性色素,广泛存在于自然界的有色物质,按化学结构可分为胡萝卜素和叶黄素两种,胡萝卜素为8个异戊二烯基本单位构成的碳氢化合物,叶黄素则是胡萝卜素的含氧衍生物[19]。光合生物体内类胡萝卜素的功能是将吸收的光能传给叶绿素,但传递效率比叶绿素间的传递效率低。藻胆素是蓝藻、红藻中一种以四吡咯环形成直链共轭体系的天然捕光色素,不含镁和叶醇链,具有重要的吸收和传递光能作用。
细胞色素(cytochrome,Cyt)与叶绿素具有类似的卟啉结构,是一类以铁卟啉(或血红素)作为辅基的电子传递蛋白,主要有Cyt a、Cyt b、Cyt c、Cyt d和Cyt o等类型,广泛参与动植物、好氧菌、厌氧光合菌等的氧化还原反应,主要负责电子传递,即细胞色素充当的是电子传递体作用。其中的Cyt c被研究得最多(图2D),它是一种血红素蛋白,是细菌或真核生物线粒体内膜电子穿梭所必需的成分,能将电子从细胞内传递到细胞外的电子受体[31-33]。细胞色素上的卟啉环以4个配位键与1个铁原子相连,形成四配位的络合物,在这样的环状体系中,铁原子处于活泼的化学状态,通过血红素辅基中铁原子的还原态(Fe2+)和氧化态(Fe3+)之间的可逆变化起到传递电子的作用,这就是细胞色素可以传递电子的原理,而电子传递是光能转化得以顺利进行的重要一环。
-
天然的溶解性有机质(dissolved organic matter, DOM)具有光催化特性,可以吸收部分紫外光以及可见光。DOM具有表面粗糙,比表面积小、孔隙率大的表面性质,在对光的吸收上有较大的优势。腐殖质(humic substance, DHS)中的腐殖酸(humic acid, HA)和富里酸(fulvic acid, FA)是典型的天然DOM。HS是一类中心由稠环或易生稠环芳核等发色基团构成的高分子复杂混合物,具有吸收光能(主要吸收280<λ<400 nm的紫外部分太阳光[34])和产生自由基的光敏化能力,在产生ROS(·OH、1O2、O2-·)以及其自身的激发三重态(3HS*)方面具有较高的活性[35-36],因此在调控天然水体中有机污染物的光化学行为上发挥着重要作用。
用于表征DOM的光化学特性的常用手段有紫外吸收光谱以及荧光激发发射光谱,表征DOM吸收光谱的参数通常包括特征紫外吸光度 (specific ultraviolet absorbance, SUVA)、特征波段的斜率S、E2/E3 (波长254 nm和365 nm的吸光度的比值)等[37],这些光化学参数分别表征不同的性质。SUVA用于表征DOM的紫外吸收光强度,研究表明,分子量大、芳香类结构多的DOM对应的SUVA值高,具有更强的光化学活性。E2/E3则用于表征DOM紫外吸收光谱特征和变化,指示DOM通过电荷转移发生光化学反应的情况,E2/E3大,表明光化学过程受电荷转移影响较小,反之影响较大,且相关研究表明,1O2的量子产率与E2/E3值呈正相关,即说明该物质具有更强的光化学氧化能力。
黑碳是化石燃料和生物质不完全燃烧的产物,在河口和海洋中大量存在。黑碳中水溶性部分称为溶解性黑碳(dissolved black carbon,DBC),同样是天然DOM中的重要组成部分[38-40]。相较其它研究较多的DOM类型,DBC具有更小的分子量。DBC中羰基含量越高,光敏反应活性越强[41]。DBC能产生多种活性氧物种,其被光激发的过程为:DBC吸收太阳光,产生三重激发态(3DBC*),3DBC*再与溶解氧反应生成1O2等ROS [42]。
-
自然硫(S0)是指斜方晶系的α硫,在火山岩中广泛存在,是一种非常丰富的矿物元素,作为一种典型的非金属半导体矿物,具有一定的光化学活性。与金属硫化物半导体矿物不同的是其吸收光主要为紫外光。S0有两个不连续带隙,其中的直接带隙为4.4 eV(VB值为2.06 eV,CB值为-2.34 eV),只能吸收紫外光(<280 nm),起主要作用,而较窄的间接带隙仅产生少量光电子,作用不大。其光催化机理是紫外光促使S0开环断键形成光电子和活性硫自由基(S·),进而通过硫自由基进行电子传递。
-
具备光催化特性的天然物质对环境产生的效应可以分为两类,一方面是天然光催化物质在光激发下产生的具有强氧化性的光生空穴、自由基以及天然光催化物质的三重态的环境效应。另一方面,天然光催化物质在光激发下产生的光生电子具有强还原性,对环境生物地球循环也产生着影响。
-
天然光催化物质在光照下产生的光生空穴、光生自由基以及天然光催化物质的三重态等,具有强氧化性,如图3所示,它们不仅具备杀菌消毒的作用,还能将天然水体和土壤中的有机污染物氧化分解为毒性小或无毒的小分子无机物[43]。叶绿素、藻胆素以及DBC等天然光催化物质均具备产生1O2的能力,叶绿素产生的1O2可以将有机污染物氧化为水和二氧化碳,对于污染治理及环境改善有重大意义。Luo等[23]发现死亡微藻在光照条件下具有降解苯并(a)芘的能力,是因为叶绿素在光照下通过光催化产生大量氧化性较强的1O2,将苯并(a)芘光氧化为醌类化合物。藻胆素和叶绿素一样具有光学活性,在光的激发下,藻蓝胆素可以产生1O2等ROS,对肿瘤等生物大分子具有杀伤力。Wang等[42]利用DBC产生的3DBC*和1O2加速了2,4,6-三甲基苯酚的降解,通过测量DBC和几种天然陆生NOM的1O2量子产率以及3DBC*量子产率可知,DBC的量子产率是天然陆生NOM量子产率的1.75倍,相应的DBC降解 2,4,6-三甲基苯酚的能力是天然陆生NOM的12倍。
·OH是一种重要的活性氧,具有极强的得电子能力即氧化能力,被认为是光催化氧化过程中的主要反应物[44]。天然光催化物质产生的·OH在降解废水中的有色染料、杀菌以及降低有机负荷发挥着重要作用。Pekakis等[45]发现二氧化钛产生的·OH对印染废水有较好的脱色及降低有机负荷的作用,且不会产生有毒有害副产物。Pan课题组Ren等 [35]证明HS光敏化产生的·OH是导致废水中炔雌醇甲醚氧化降解的主要原因。 Borges等[13] 发现负载在天然矿物(黑色熔岩火山灰)上的TiO2在可见光下是一种高效的光催化剂,仅需光照2 h,废水中污染物的降解率可达 95%,其产生的·OH是这个反应中主要的ROS,表明该材料可用于处理高浓度废水的光反应器中。在杀菌效应方面,MacFarlane等[46]发现TiO2表面对铜绿假单胞菌、金黄色葡萄球菌和白色念珠菌细胞有较高的杀灭效果,主要是由于光照下TiO2与表面的水分子相互作用产生的·OH将微生物的细胞膜氧化。Dukan等[47]证明了TiO2的杀菌机理是光照下产生·OH对细菌细胞的DNA造成损伤。
天然物质在光催化过程中产生的O2-· 和 h+也有重要的环境效应,Zhou等[48]证明CdS与微生物耦合的混合系统在光照条件下能够产生O2-·等ROS抑制敏感的N2O还原酶,从而抑制N2O的还原,导致N2O大量排放,由此找到一种从废水中回收N2O的低成本可持续的方法。
天然光催化物质的三重态,如3DBC*和3HS*,具有较强的氧化能力,在水生环境的生物地球化学以及调控天然水体中的有机污染物的光化学行为上发挥着重要作用[49]。三重态是指自旋多重度等于三的量子态,大部分天然光催化物质的分子基态是处于单重态的,但在电子跃迁过程中,可能伴随着电子自旋的改变,此时两个电子的自旋方向相同,形成三重激发态。Pan课题组Ren等[35]发现HS介导炔雌醇甲醚光转化过程中除了·OH起主要作用外,其三重激发态3HS*对炔雌醇甲醚的氧化也有一定贡献。Carlos课题组[50]研究了在HS存在的情况下各种新兴污染物的光降解,其中对乙酰氨基酚和卡马西平的间接光解最为明显,并通过淬灭反应证明了这种间接光解主要是由HS的三重激发态介导的氧化作用引起的。Zhou等[39]证明, DBC在光激发下产生的3DBC*能促进17β-雌二醇的光降解。且在相同碳浓度下,DBC介导的17β-雌二醇光转化的表观量子产率约为HS的6倍。
-
天然光催化物质能吸收大于自身禁带宽度的光能从而生成强还原性的光电子(图3),鲁安怀教授团队认为,这种由天然光催化物质发生光电效应产生的光电子能量,是自然界中继太阳光子能量和元素价电子能量之后的第三种重要能量形式[18]。目前的研究已发现,天然光催化物质产生的光电子可以驱动非光合微生物的固碳和固氮等生长代谢活动、促进环境中重金属及有机污染物的还原、促进微生物细胞间电子传递,还可直接驱动地球碳氮元素循环中的化学还原反应。
天然光催化物质产生的光电子能促进微生物介导的碳氮循环反应。例如Li等[51]发现非光能化合自养菌Acidithiobacillus ferrooxidans能以天然矿物金红石(主要成分为TiO2)产生的光电子为能量来源,提高CO2转化为有机碳的效率。自然光合作用固定CO2的速率远不及自然界中其它反应生成CO2的速率,近年来半导体-微生物杂化体系的人工光合作用被研究得越来越多,该类体系旨在模拟由太阳能驱动的将CO2转化为增值碳产品的过程[52-53]。杨培东教授[54]构建的非光合微生物-半导体(Moorella thermoacetica–CdS)杂化体系在光照下能将CO2还原为CH3COOH,CdS吸收光能,激发出光电子,M. thermoacetica利用光电子进行光合成。这种由光电子驱动的非光合微生物发生半人工光合作用的效率与自然光合作用相当。Ye等[55]构建的Methanosarcina barkeri-CdS半人工光合体系具有还原CO2为CH4的功能。用不同剂量蛋白酶K将膜结合蛋白消化,实验数据表明,随着蛋白酶K剂量的增加,该体系产CH4的能力逐渐降低,证明M. barkeri上的膜结合蛋白在光电子传递过程中起关键作用。其电子传递机制可总结为光照下光生载流子(e―-h+)分离,电子进入外膜蛋白用于CO2还原。在微生物氮循环方面,Chen等[56]利用化能自养菌Thiobacillus denitrificans和CdS构建的体系,将NO3-还原为N2O。CdS受光激发产生的电子是脱氮硫杆菌还原NO3-的主要电子源,其电子转移路径为:CdS产生的电子通过Thiobacillus denitrificans外膜上的电子受体,如c型细胞色素等传递到细胞内,然后通过一系列电子转移链传递到反硝化酶中,促进NO3-的还原,黄绍福等[57] 构建了Pseudomonas stutzeri-CdS半人工光合系统驱动微生物固氮,该系统具有捕获光能并还原N2成NH3能力。光照时,P.stutzeri可以利用CdS产生的光电子促进固氮酶基因的表达,从而促进胞内N2还原成NH3过程。
在污染物降解转化方面,光照下,希瓦氏菌—赤铁矿的协同作用能够将Cr(Ⅵ)还原为Cr(Ⅲ)。这种还原机制涉及两条电子传递路径,一方面,希瓦氏菌通过代谢电子供体乳酸盐生成的一部分电子将Cr(Ⅵ)还原,Zhu等[58]这类电子称为生物电子。另一方面,另一部分生物电子填补赤铁矿产生的空穴,促进光生空穴-电子对的分离,从而产生更高的电流输出,这部分光生电子同样具有将Cr(Ⅵ)还原为Cr(Ⅲ)的能力,两条路径结合大大提升了Cr(Ⅵ)的还原效率。此外,天然细胞色素P450 119(CYP119)在光照下没有还原Cr(Ⅵ)的能力,但与半导体复合物CeO2-3TiO2偶联时,会表现出较强的光催化活性。表明光催化物质除了能驱动微生物的反应,也能驱动色素蛋白的还原反应[15]。天然金属硫化物如CdS、ZnIn2S4等在光照条件下催化还原有毒、强腐蚀性气体H2S以制氢,实现H2S的转移和清洁能源H2的产生[59]。Huang等[60]构建Geobacter sulfurreducens-CdS杂化体系,光照下, G. sulfurreducens能以CdS产生的光电子为唯一电子供体还原偶氮染料甲基橙,在3 h时,甲基橙的去除率达到100%,相比黑暗对照组,去除速率提高了8倍以上。CdS在光激发下产生的光电子先储存在G. sulfurreducens的外膜细胞色素c(外膜蛋白OmcB)中,然后转移到末端还原酶降解甲基橙。
光催化物质产生的光电子能促进具备胞外电子传递能力的电活性微生物的生长。Chen等[56] 发现可见光会抑制Geobacter metallireducens与G. sulfurreducens共培养的形成。而添加CdS可以缓解这种Geobacter共培养体系中的光胁迫现象,原因是光照下CdS产生的光电子可驱动Geobacter种间电子传递,与没有CdS的对照组相比,光电子参与的种间电子传递过程减少了对Geobacter合成Gmet_2896和OmcS细胞色素的需求,因而减少了整个过程中用于细胞色素生物合成的能量消耗,从而缓解了光胁迫效应。此外,天然光催化物质能为具备胞外电子传递能力的电活性微生物提供电子供体作为能量,因此能促进电活性微生物的生长,增加电活性微生物在环境中的丰度,Ren等[61]对新疆戈壁沙漠岩漆的矿物组成及细菌群落分布进行分析,发现在岩漆矿物越多的地方,群落中电活性微生物的比例越大。
除作用于微生物外,光电子还可直接作用于化学还原反应。鲁安怀课题组Li等[62]研究了S0的光电化学性质,发现腾冲热泉中的自然硫在紫外光辐射下产生高能量光电子直接将大气中CO2还原成HCOOH,这种无机碳向有机碳的转换仅发生在含自然硫体系中,这一发现解开了陆地热泉系统生命起源之谜。
综合以上环境效应,可得知:
(1)目前发现的天然光催化物质产生的具有强氧化性的光生空穴/自由基的环境效应主要包括两大方面,一方面是将天然水体和土壤中的复杂有机污染物氧化分解为毒性小或无毒的小分子无机物,这些有机污染物包括苯并(a)芘、2,4,6-三甲基苯酚、炔雌醇甲醚、乙酰氨基酚、卡马西平以及17β-雌二醇等。另一方面体现在天然光催化物质产生的强氧化性自由基的杀菌消毒,尤其对铜绿假单胞菌、金黄色葡萄球菌和白色念珠菌有较强的杀伤作用。
(2)目前发现的天然光催化物质产生的具有强还原性的电子的环境效应主要包括两大方面,一方面是对有毒有害无机物的还原,包括CO2、NO3-、N2、Cr(Ⅵ)、H2S等,对这些物质的还原不仅减轻了环境的负荷,还促进了地球生物化学的有益循环。另一方面体现在天然矿物在光的激发下促进微生物细胞间电子传递,驱动电活性微生物的生长。
可以看出,研究天然光催化物质的生态学和环境学意义在近几年受到广泛关注,为理解水体以及土壤中碳、氮循环、有机污染物的迁移转化等关键生物地球化学过程提供了全新的科学视角。但在处理环境问题方面,目前天然光催化物质产生的具有氧化性的光生空穴/自由基主要处理的是有机污染物,对无机污染物涉及较少。而天然光催化物质产生的具有还原性的电子主要处理的是有毒有害的无机物,对有机污染物的迁移转化效果相比而言不及无机污染物。相信在未来的研究中,能够挖掘更多具备高效光催化性能的天然物质,减小处理环境问题的局限性。
-
天然光催化物质的光电特性与环境效应在近年逐渐被挖掘,本文主要综述了具有光催化性能的天然物质及其环境效应。首先,介绍了表征光催化性能的参数(如价带、导带、带隙和光电流密度),并说明其如何表征光催化性能。其次,阐述了天然金属矿物、天然色素、天然溶解有机物和自然硫4类典型的天然光催化物质及其光催化机理,介绍了以金属硫化物和金属氧化物为主的天然金属矿物的基本光催化参数和光催化原理;天然色素(叶绿素、类胡萝卜素、藻胆素和细胞色素)的类型和结构特征;典型的天然溶解有机物、腐殖质和溶解黑碳的光催化特性和三重态的生成;以及作为典型非金属半导体矿物的自然硫的光化学活性。最后,从强氧化性的光生空穴/自由基和强还原性的光生电子两个方面阐述了上述4种天然物质的环境效应。虽然说天然物质的光催化特性是近年来生态、生物、能源和环保领域的研究热点,但目前相关的科研工作尚处于起步阶段,未来可从下列方向进行广度或深度的拓展:
(1)长期以来,研究者们关注的天然光催化物质仅有金属矿物和有机质,自然硫的光电特性直至2020年才被深入认识,更多的天然光催化物质类型有待被发现。此外,在效应研究部分,光电子对生命起源与演化、地球生物化学循环具有重要意义,然而目前对光生电子的生成机制和效应研究主要集中在天然金属矿物类物质,关于其它类型天然光催化物质的光生电子机制与效应的报道十分匮乏,未来应继续挖掘潜在的天然光催化物质类型,拓宽并加深天然光催化物质的机制与效应研究。
(2)目前所涉及到的天然光催化物质产生的光生自由基、光生空穴以及光生电子的环境效应大部分基于实验室条件进行探究,如研究水体或土壤表层光生自由基时,通常需要将水样或土样投加到含苯甲酸钠、5,5-二甲基-1-吡咯啉-N-氧化物等自由基捕获剂的溶液中,再进行液体采样,然后用液相色谱或电子顺磁共振波谱仪进行测定,在野外原位测定的研究较少。野外环境存在许多影响光电效应的天然空穴捕获剂、天然电子介体和光能竞争体等,复杂程度有别于实验室,如何真实反映天然光催化物质在实际自然环境中的效应有待进一步探索。而进行野外实验探索的先决条件是研发便于原位快速测定光生自由基、光生空穴以及光生电子的方法与设备,如微电极、荧光探针、化学发光法和电化学生物传感器等,并转化为实际可用的产品。
(3)人工合成的光催化物质吸收波段通常比较单一,而某些天然光催化物质如色素类等的可吸收波段广,因此在光能利用效率上具有优势。在往后的研究中,可研发天然光催化物质-人工光催化物质杂化材料,或依据天然光催化物质的光吸收原理研发仿生类光催化材料,从而达到耦合人工光催化物质光电效率高和天然光催化物质光能利用效率高两大优势的目的,优化光催化技术的应用范围与效果。
天然光催化物质的光电特性与环境效应研究进展
Advances in photoelectric properties and environmental effects of natural photocatalytic substances
-
摘要: 自然界中存在许多天然光催化物质,它们对驱动地球生物化学循环产生着不可忽视的影响,挖掘绿色天然的光催化物质无论是在环境效益还是经济效益上都具有重要意义。本文总结了目前已发现的自然界中具有光催化性能的天然物质,介绍其光催化特性的表征方法,重点阐述天然金属矿物、天然色素、天然溶解性有机质及天然硫四类物质的光催化特性及原理,从强氧化性的光生空穴/自由基及强还原性的光生电子的角度探讨天然光催化物质在驱动非光合微生物生长代谢、加速污染物降解转化、促进电活性微生物生长等方面的效应与机制,并从效应研究和工程应用的角度展望其今后的发展方向。Abstract: There are many natural photocatalytic substances in nature, which play an important role in driving the biochemical cycle of the earth. The excavation of green natural photocatalytic substances is of great significance in both environmental and economic benefits. This paper mainly reviews the natural substances with photocatalytic properties and introduces the characterization methods of their photocatalytic properties, focusing on the photocatalytic characteristics and principles of four natural substances including the metal mineral, the natural pigment, the natural dissolved organic matter and the natural sulfur. We discuss the effects and mechanisms of natural photocatalytic substances in driving the growth and metabolism of non-photosynthetic microorganisms, accelerating the degradation and transformation of pollutants, and promoting the growth of electroactive microorganisms from perspectives of strongly oxidizing photogenerated holes/free radicals and strongly reducing photogenerated electrons. The future development directions from the point of view of effect research and engineering application are proposed.
-
Key words:
- natural substance /
- photocatalysis /
- photogenerated free radical /
- photoelectron /
- environmental effect
-

-
物质
Materials价带/eV
Valence band导带/eV
Conduction band波长/nm
Wavelength分布
Distribution
金属氧化物锐钛矿(TiO2) 2.54 −0.66 387 火成岩及变质岩矿脉 赤铁矿(Fe2O3) 2.48 0.28 565 火成岩 斜锆石(ZrO2) 3.91 −1.09 249 碳酸岩矿床或砂矿 黑锡矿(SnO) 3.29 −0.91 296 热液矿床 褐铊矿(Tl2O3) 1.65 0.05 777 天然河流重砂 铅黄(PbO) 2.32 −0.48 444 硫化物矿床的氧化带 金属硫化物 闪锌矿(ZnS) 2.56 −1.04 345 热液矿床 硫镉矿(CdS) 1.88 −0.52 518 铅锌矿床氧化带 辰砂(HgS) 2.02 0.02 622 低温热液矿床 红铊矿(TlAsS2) 1.46 −0.34 691 天然河流重砂 辉钨矿(WS2) 1.71 0.36 921 脉钨矿床 类别
Category主要结构
Main structure吸收波长/nm
Absorption wavelength分布
Distribution叶绿素 叶绿素a 镁卟啉环 420—440、660—680 所有绿色植物 叶绿素b 460—480、640—650 高等植物、绿藻等 叶绿素c 460—475、620—640 硅藻、甲藻、褐藻等 叶绿素d 700—750 红藻、蓝藻 叶绿素f 700—800 藻青菌 细菌叶绿素 715—1050 各种厌氧光合细菌 类胡萝卜素 胡萝卜素 8个异戊二烯相连 430-480 藻类、真菌、细菌、高等植物 叶黄素 藻胆素 藻蓝胆素 线性四吡咯 640 蓝藻、红藻等 藻红胆素 550 藻紫胆素 590 藻尿胆素 490 细胞色素 铁卟啉环 450 嗜酸古生菌 -
[1] SPASIANO D, MAROTTA R, MALATO S, et al. Solar photocatalysis: Materials, reactors, some commercial, and pre-industrialized applications. A comprehensive approach [J]. Applied Catalysis B:Environmental, 2015, 170/171: 90-123. doi: 10.1016/j.apcatb.2014.12.050 [2] LACOMBE S, KELLER N. Photocatalysis: Fundamentals and applications in JEP 2011 [J]. Environmental Science and Pollution Research, 2012, 19(9): 3651-3654. doi: 10.1007/s11356-012-1040-8 [3] LIU B S, WU H, PARKIN I P. New insights into the fundamental principle of semiconductor photocatalysis [J]. ACS Omega, 2020, 5(24): 14847-14856. doi: 10.1021/acsomega.0c02145 [4] KUMAR V, SINHA A, FAROOQUE U. Concentration and temperature dependence of the energy gap in some binary and alloy semiconductors [J]. Infrared Physics & Technology, 2015, 69: 222-227. [5] OKAZAKI S, TOMO T, MIMURO M. Direct measurement of singlet oxygen produced by four chlorin-ringed chlorophyll species in acetone solution [J]. Chemical Physics Letters, 2010, 485(1/2/3): 202-206. [6] IBHADON A, FITZPATRICK P. Heterogeneous photocatalysis: Recent advances and applications [J]. Catalysts, 2013, 3(1): 189-218. doi: 10.3390/catal3010189 [7] PARRINO F, LODDO V, AUGUGLIARO V, et al. Heterogeneous photocatalysis: Guidelines on experimental setup, catalyst characterization, interpretation, and assessment of reactivity [J]. Catalysis Reviews, 2019, 61(2): 163-213. doi: 10.1080/01614940.2018.1546445 [8] LU A H, LI Y, DING H R, et al. Photoelectric conversion on Earth's surface via widespread Fe- and Mn-mineral coatings [J]. PNAS, 2019, 116(20): 9741-9746. doi: 10.1073/pnas.1902473116 [9] 鲁安怀, 李艳, 王鑫, 等. 关键带中天然半导体矿物光电子的产生与作用 [J]. 地学前缘, 2014, 21(3): 256-264. doi: 10.13745/j.esf.2014.03.027 LU A H, LI Y, WANG X, et al. The photoelectron generation from semiconducting minerals and its effects in critical zone [J]. Earth Science Frontiers, 2014, 21(3): 256-264(in Chinese). doi: 10.13745/j.esf.2014.03.027
[10] SHANG J, HAO W C, LV X, et al. Bismuth oxybromide with reasonable photocatalytic reduction activity under visible light [J]. ACS Catalysis, 2014, 4(3): 954-961. doi: 10.1021/cs401025u [11] 任桂平, 孙曼仪, 鲁安怀, 等. 纳米赤铁矿电极光电催化特性及苯酚降解活性研究 [J]. 岩石矿物学杂志, 2017, 36(6): 825-832. doi: 10.3969/j.issn.1000-6524.2017.06.007 REN G P, SUN M Y, LU A H, et al. Photoelectrochemical performance of nano-hematite electrode and photoelectrocatalytic activity toward oxidation of phenol [J]. Acta Petrologica et Mineralogica, 2017, 36(6): 825-832(in Chinese). doi: 10.3969/j.issn.1000-6524.2017.06.007
[12] LIU J H, YANG R, LI S M. Preparation and characterization of high photoactive TiO2 catalyst using the UV irradiation-induced Sol-gel method [J]. Journal of University of Science and Technology Beijing, Mineral, Metallurgy, Material, 2006, 13(4): 350-354. doi: 10.1016/S1005-8850(06)60072-8 [13] BORGES M E, SIERRA M, CUEVAS E, et al. Photocatalysis with solar energy: Sunlight-responsive photocatalyst based on TiO2 loaded on a natural material for wastewater treatment [J]. Solar Energy, 2016, 135: 527-535. doi: 10.1016/j.solener.2016.06.022 [14] JIANG Z F, SUN H L, WANG T Q, et al. Nature-based catalyst for visible-light-driven photocatalytic CO2 reduction [J]. Energy & Environmental Science, 2018, 11(9): 2382-2389. [15] JIANG H L, LI X Q, LI M L, et al. A new strategy for triggering photocatalytic activity of Cytrochrome P450 by coupling of semiconductors [J]. Chemical Engineering Journal, 2019, 358: 58-66. doi: 10.1016/j.cej.2018.09.199 [16] 鲁安怀, 李艳, 丁竑瑞, 等. 地表“矿物膜”: 地球“新圈层” [J]. 岩石学报, 2019, 35(1): 119-128. doi: 10.18654/1000-0569/2019.01.08 LU A H, LI Y, DING H R, et al. “Mineral membrane” of the surface: “New sphere” of the Earth [J]. Acta Petrologica Sinica, 2019, 35(1): 119-128(in Chinese). doi: 10.18654/1000-0569/2019.01.08
[17] 鲁安怀, 李艳, 丁竑瑞, 等. 天然矿物光电效应: 矿物非经典光合作用 [J]. 地学前缘, 2020, 27(5): 179-194. LU A H, LI Y, DING H R, et al. Natural mineral photoelectric effect: Non-classical mineral photosynthesis [J]. Earth Science Frontiers, 2020, 27(5): 179-194(in Chinese).
[18] 鲁安怀, 李艳, 丁竑瑞, 等. 矿物光电子能量及矿物与微生物协同作用 [J]. 矿物岩石地球化学通报, 2018, 37(1): 1-15,158. doi: 10.19658/j.issn.1007-2802.2018.37.011 LU A H, LI Y, DING H R, et al. Mineralogical photoelectrons and minerals and microorganisms synergistic interactions [J]. Bulletin of Mineralogy, Petrology and Geochemistry, 2018, 37(1): 1-15,158(in Chinese). doi: 10.19658/j.issn.1007-2802.2018.37.011
[19] 靳青, 毕宇霖, 刘晓牧, 等. 类胡萝卜素代谢及功能研究进展 [J]. 动物营养学报, 2014, 26(12): 3561-3571. doi: 10.3969/j.issn.1006-267x.2014.12.003 JIN Q, BI Y L, LIU X M, et al. Recent advances on research of carotenoid metabolism and functions [J]. Chinese Journal of Animal Nutrition, 2014, 26(12): 3561-3571(in Chinese). doi: 10.3969/j.issn.1006-267x.2014.12.003
[20] 吴志强, 周韦. 叶绿素的类别概述 [J]. 生物学通报, 2014, 49(9): 12-14. WU Z Q, ZHOU W. An overview of the categories of chlorophyl [J]. Bulletin of Biology, 2014, 49(9): 12-14(in Chinese).
[21] 马丞博. 藻蓝胆素的制备及其作为光敏剂的初步研究[D]. 烟台: 烟台大学, 2020. MA C B. Preparation of phycocyanobilin and its preliminary study as photosensitizer[D]. Yantai: Yantai University, 2020(in Chinese).
[22] GIBBONS D, FLANAGAN K J, POUNOT L, et al. Structure and conformation of photosynthetic pigments and related compounds. 15. Conformational analysis of chlorophyll derivatives - implications for hydroporphyrins in vivo [J]. Photochemical & Photobiological Sciences, 2019, 18(6): 1479-1494. [23] LUO L J, LAI X Y, CHEN B W, et al. Chlorophyll catalyse the photo-transformation of carcinogenic benzo[a]Pyrene in water [J]. Scientific Reports, 2015, 5(1): 12776. doi: 10.1038/srep12776 [24] CHEN M. Chlorophyll modifications and their spectral extension in oxygenic photosynthesis [J]. Annual Review of Biochemistry, 2014, 83: 317-340. doi: 10.1146/annurev-biochem-072711-162943 [25] 张珠, 姜齐永, 李家柱, 等. 叶绿素类四吡咯大环分子的重排反应[J]. 化学进展, 2017, 29(增刊2): 262-284. ZHANG Z, JIANG Q Y, LI J Z, et al. Rearrangement reactions of chlorophyllous tetrapyrrole macrocyclic molecules[J]. Progress in Chemistry, 2017, 29(Sup 2): 262-284(in Chinese).
[26] POSPÍŠIL P. Production of reactive oxygen species by photosystem II as a response to light and temperature stress [J]. Frontiers in Plant Science, 2016, 7: 1950. [27] TRIANTAPHYLIDÈS C, HAVAUX M. Singlet oxygen in plants: Production, detoxification and signaling [J]. Trends in Plant Science, 2009, 14(4): 219-228. doi: 10.1016/j.tplants.2009.01.008 [28] PIBIRI I, BUSCEMI S, PALUMBO PICCIONELLO A, et al. Photochemically produced singlet oxygen: Applications and perspectives [J]. ChemPhotoChem, 2018, 2(7): 535-547. doi: 10.1002/cptc.201800076 [29] ALVEY R M, BISWAS A, SCHLUCHTER W M, et al. Attachment of noncognate chromophores to CpcA of Synechocystis sp PCC 6803 and Synechococcus sp PCC 7002 by heterologous expression in Escherichia coli. [J]. Biochemistry, 2011, 50(22): 4890-4902. doi: 10.1021/bi200307s [30] BLOT N, WU X J, de THOMAS J C, et al. Phycourobilin in trichromatic phycocyanin from oceanic cyanobacteria is formed post-translationally by a phycoerythrobilin lyase-isomerase [J]. Journal of Biological Chemistry, 2009, 284(14): 9290-9298. doi: 10.1074/jbc.M809784200 [31] PINTO I F D, CHAVES-FILHO A D B, CUNHA D D, et al. Cytochrome c modification and oligomerization induced by cardiolipin hydroperoxides in a membrane mimetic model [J]. Archives of Biochemistry and Biophysics, 2020, 693: 108568. doi: 10.1016/j.abb.2020.108568 [32] ZHANG B, CHENG H Y, WANG A J. Extracellular electron transfer through visible light induced excited-state outer membrane C-type cytochromes of Geobacter sulfurreducens [J]. Bioelectrochemistry, 2021, 138: 107683. doi: 10.1016/j.bioelechem.2020.107683 [33] ZENG Y, ZHOU X, QI R L, et al. Photoactive conjugated polymer-based hybrid biosystems for enhancing cyanobacterial photosynthesis and regulating redox state of protein [J]. Advanced Functional Materials, 2021, 31(8): 2007814. doi: 10.1002/adfm.202007814 [34] 刘砚弘. 溶解性有机质及其与铁共存时的光化学活性研究[D]. 南京: 南京林业大学, 2019. LIU Y H. Research on photochemical activity of dissolved organic matter and its coexistence with iron[D]. Nanjing: Nanjing Forestry University, 2019(in Chinese).
[35] REN D, HUANG B, YANG B Q, et al. Mitigating 17α-ethynylestradiol water contamination through binding and photosensitization by dissolved humic substances [J]. Journal of Hazardous Materials, 2017, 327: 197-205. doi: 10.1016/j.jhazmat.2016.12.054 [36] BODHIPAKSHA L C, SHARPLESS C M, CHIN Y P, et al. Triplet photochemistry of effluent and natural organic matter in whole water and isolates from effluent-receiving rivers [J]. Environmental Science & Technology, 2015, 49(6): 3453-3463. [37] 刘雪石, 乔显亮, 刘远. DOM的光化学活性及其对污染物光解的影响 [J]. 环境科学与技术, 2017, 40(1): 85-94. LIU X S, QIAO X L, LIU Y. Photoreactivity of DOM and its effect on the photo-transformation of pollutants [J]. Environmental Science & Technology, 2017, 40(1): 85-94(in Chinese).
[38] DU Z Y, HE Y S, FAN J N, et al. Predicting apparent singlet oxygen quantum yields of dissolved black carbon and humic substances using spectroscopic indices [J]. Chemosphere, 2018, 194: 405-413. doi: 10.1016/j.chemosphere.2017.11.172 [39] ZHOU Z C, CHEN B N, QU X L, et al. Dissolved black carbon as an efficient sensitizer in the photochemical transformation of 17β-estradiol in aqueous solution [J]. Environmental Science & Technology, 2018, 52(18): 10391-10399. [40] QI Y Z, FU W J, TIAN J W, et al. Dissolved black carbon is not likely a significant refractory organic carbon pool in rivers and oceans [J]. Nature Communications, 2020, 11: 5051. doi: 10.1038/s41467-020-18808-8 [41] TIAN Y J, FENG L, WANG C, et al. Dissolved black carbon enhanced the aquatic photo-transformation of chlortetracycline via triplet excited-state species: The role of chemical composition [J]. Environmental Research, 2019, 179: 108855. doi: 10.1016/j.envres.2019.108855 [42] WANG H, ZHOU H X, MA J Z, et al. Triplet photochemistry of dissolved black carbon and its effects on the photochemical formation of reactive oxygen species [J]. Environmental Science & Technology, 2020, 54(8): 4903-4911. [43] NOSAKA Y, NOSAKA A Y. Generation and detection of reactive oxygen species in photocatalysis [J]. Chemical Reviews, 2017, 117(17): 11302-11336. doi: 10.1021/acs.chemrev.7b00161 [44] NOSAKA Y, NOSAKA A. Understanding hydroxyl radical (•OH) generation processes in photocatalysis [J]. ACS Energy Letters, 2016, 1(2): 356-359. doi: 10.1021/acsenergylett.6b00174 [45] PEKAKIS P A, XEKOUKOULOTAKIS N P, MANTZAVINOS D. Treatment of textile dyehouse wastewater by TiO2 photocatalysis [J]. Water Research, 2006, 40(6): 1276-1286. doi: 10.1016/j.watres.2006.01.019 [46] MACFARLANE J W, JENKINSON H F, SCOTT T B. Sterilization of microorganisms on jet spray formed titanium dioxide surfaces [J]. Applied Catalysis B:Environmental, 2011, 106(1/2): 181-185. [47] GOGNIAT G, DUKAN S. TiO2 photocatalysis causes DNA damage via Fenton reaction-generated hydroxyl radicals during the recovery period [J]. Applied and Environmental Microbiology, 2007, 73(23): 7740-7743. doi: 10.1128/AEM.01079-07 [48] CHEN M, ZHOU X F, CHEN X Y, et al. Mechanisms of nitrous oxide emission during photoelectrotrophic denitrification by self-photosensitized Thiobacillus denitrificans [J]. Water Research, 2020, 172: 115501. doi: 10.1016/j.watres.2020.115501 [49] SHARPLESS C M, AESCHBACHER M, PAGE S E, et al. Photooxidation-induced changes in optical, electrochemical, and photochemical properties of humic substances [J]. Environmental Science & Technology, 2014, 48(5): 2688-2696. [50] CARLOS L, MÁRTIRE D O, GONZALEZ M C, et al. Photochemical fate of a mixture of emerging pollutants in the presence of humic substances [J]. Water Research, 2012, 46(15): 4732-4740. doi: 10.1016/j.watres.2012.06.022 [51] LI Y, LU A H, WANG X, et al. Semiconducting mineral photocatalytic regeneration of Fe2+Promotes carbon dioxide acquisition by Acidithiobacillus ferrooxidans [J]. Acta Geologica Sinica - English Edition, 2013, 87(3): 761-766. doi: 10.1111/1755-6724.12087 [52] KIM D, SAKIMOTO K K, HONG D C, et al. Artificial photosynthesis for sustainable fuel and chemical production [J]. Angewandte Chemie (International Ed. in English), 2015, 54(11): 3259-3266. doi: 10.1002/anie.201409116 [53] CESTELLOS-BLANCO S, ZHANG H, KIM J M, et al. Photosynthetic semiconductor biohybrids for solar-driven biocatalysis [J]. Nature Catalysis, 2020, 3(3): 245-255. doi: 10.1038/s41929-020-0428-y [54] SAKIMOTO K K, WONG A B, YANG P D. Self-photosensitization of nonphotosynthetic bacteria for solar-to-chemical production [J]. Science, 2016, 351(6268): 74-77. doi: 10.1126/science.aad3317 [55] YE J, YU J, ZHANG Y Y, et al. Light-driven carbon dioxide reduction to methane by Methanosarcina barkeri-CdS biohybrid [J]. Applied Catalysis B:Environmental, 2019, 257: 117916. doi: 10.1016/j.apcatb.2019.117916 [56] CHEN M, ZHOU X F, YU Y Q, et al. Light-driven nitrous oxide production via autotrophic denitrification by self-photosensitized Thiobacillus denitrificans [J]. Environment International, 2019, 127: 353-360. doi: 10.1016/j.envint.2019.03.045 [57] 黄绍福, 靖宪月, 陈曼, 等. 光驱动Pseudomonas stutzeri-CdS半人工光合系统固氮产氨效果与机制 [J]. 中国科学:技术科学, 2021, 51(4): 435-445. doi: 10.1360/SST-2020-0238 HUANG S F, JING X Y, CHEN M, et al. Feasibility and mechanism of light-driven nitrogen reduction to ammonium by a Pseudomonas stutzeri-CdS semi-artificial photosynthetic system [J]. Scientia Sinica (Technologica), 2021, 51(4): 435-445(in Chinese). doi: 10.1360/SST-2020-0238
[58] ZHU G L, YANG Y, LIU J, et al. Enhanced photocurrent production by the synergy of hematite nanowire-arrayed photoanode and bioengineered Shewanella oneidensis MR-1 [J]. Biosensors & Bioelectronics, 2017, 94: 227-234. [59] 淡猛, 蔡晴, 向将来, 等. 用于光催化分解硫化氢制氢的金属硫化物 [J]. 化学进展, 2020, 32(7): 917-926. DAN M, CAI Q, XIANG J L, et al. Metal sulfide semiconductors for photocatalytic hydrogen production from waste hydrogen sulfide [J]. Progress in Chemistry, 2020, 32(7): 917-926(in Chinese).
[60] HUANG S F, TANG J H, LIU X, et al. Fast light-driven biodecolorization by a Geobacter sulfurreducens–CdS biohybrid [J]. ACS Sustainable Chemistry & Engineering, 2019, 7(18): 15427-15433. [61] REN G P, YAN Y C, NIE Y, et al. Natural extracellular electron transfer between semiconducting minerals and electroactive bacterial communities occurred on the rock varnish [J]. Frontiers in Microbiology, 2019, 10: 293. doi: 10.3389/fmicb.2019.00293 [62] LI Y Z, LI Y, LIU Y, et al. Photoreduction of inorganic carbon(+IV) by elemental sulfur: Implications for prebiotic synthesis in terrestrial hot springs [J]. Science Advances, 2020, 6(47): 3687. doi: 10.1126/sciadv.abc3687 -




 下载:
下载: