-
生物处理法由于其成本低、效率高等优势被广泛应用于生活污水处理[1],污水中的有机物与各种营养物质(氮、磷等)通过微生物代谢被利用。其中,温度和碳源是影响该过程的重要因素[2]。低温会使微生物活性和底物利用率下降,导致污水处理性能下降[3];另一方面,低温也会导致活性污泥的沉降性能变差,出现污泥膨胀[4]。有机碳源是微生物反硝化过程的电子供体和能源,碳源缺乏会对脱氮造成不利影响[5]。
A2/O工艺具有工艺流程简单、运行灵活、水力停留时间短、活性污泥不易膨胀、基建和运行费用低等优点[6],因而在国内外应用广泛。但A2/O工艺本身就存在反硝化菌与聚磷菌的碳源竞争等矛盾,在低碳氮比的进水条件下,这一矛盾愈发突出。低温条件下,A2/O工艺的启动受到显著负面影响,生物处理系统的效率明显下降[7]。
在我国大部分地区的城市生活污水,尤其是南方地区的城市生活污水,均具有C/N偏低的特点,COD一般约为200 mg·L−1[8],COD/TN为3.3~8.5[9],而满足或完成反硝化的COD/TN为4~15[8]。在温度方面,由于地理区域的差异以及季节变化,水温可能降低至8~15 ℃,甚至低于5 ℃[3]。因此,低温低C/N的进水条件对污水生物处理系统的稳定运行和生物脱氮的效率提出了挑战。
基于上述研究,本研究利用中试规模的A2/O装置,研究了低温低C/N进水条件下装置的脱氮规律,并结合反应动力学,评估了该条件对脱氮效果的影响,以期为优化低温低C/N进水条件下A2/O工艺的运营调控提供数据支持。
全文HTML
-
本实验接种的污泥取自北京市清河污水处理厂。装置进满污水后,停止进水,接种浓缩污泥后持续曝气,至污泥转为黄褐色时开始进水(进水量逐步增加),将外循环系统打开,让污泥在装置内循环。待污泥具备良好的沉降性能与表观特性时,即标志污泥驯化完成。
-
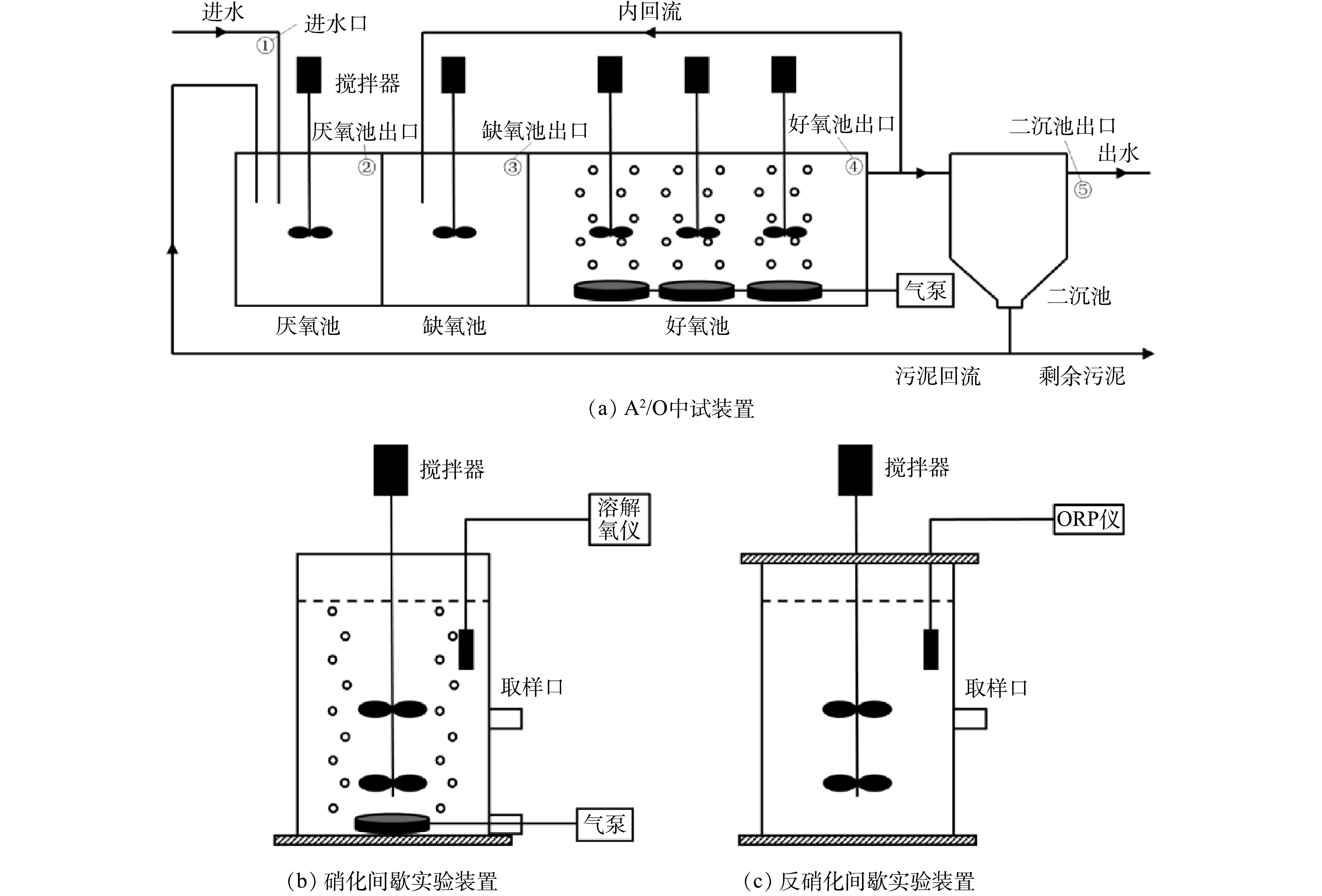
1)A2/O中试装置与运行参数。本研究使用的实验装置见图1。A2/O中试装置如图1(a)所示。装置主体规格为2 660 mm×400 mm×550 mm,有效容积为480 L,V厌氧池∶V缺氧池∶V好氧池为1∶1∶3,总水力停留时间(HRT)为12 h,污泥龄(SRT)为15 d,污泥回流比r为100%,混合液回流比R为250%。
实验用水取自中国人民大学总排水口排放的实际生活污水。由于取水口位于宿舍区与食堂附近,原水浓度较高。为模拟我国普遍存在的生活污水COD较低、C/N低的特点,用自来水对原水进行1∶1的稀释。其水质情况见表1。其中,COD的平均值为199.0 mg·L−1,COD/TN为4.43,为典型的低C/N进水。在实验期间,水温为11.3~15.5 ℃,平均为12.73 ℃,进水流量Q为1.02 m3·d−1,污泥负荷为0.23 kg·(kg·d)−1(以COD计),污泥的质量浓度(MLSS)为2 300~3 000 mg·L−1。
2)反应动力学实验装置与运行参数。反应动力学实验采用SBR装置进行,硝化实验装置如图1(b)所示,反硝化实验装置如图1(c)所示。实验使用的活性污泥(体积为8 L)分别取自A2/O中试装置的好氧池和缺氧池,在SBR装置中静置沉淀30 min,将上清液排出,注入等体积的清水后再次静置沉淀30 min,排出上清液,最后补入等体积的人工配水,开始生化反应。
-
1)水质指标。本实验测试的水质指标为COD、
$ {\rm{NH}}_4^ + $ -N、${\rm{NO}}_3^ - $ -N、${\rm{NO}}_2^ - $ -N、TN等,均按照《水和废水监测分析方法(第4版)》中的标准方法进行分析。其中,COD采用快速消解法测定;$ {\rm{NH}}_4^ + $ -N采用纳氏试剂光度法测定;${\rm{NO}}_3^ - $ -N采用紫外分光光度法测定;${\rm{NO}}_2^ - $ -N采用N-(1-萘基)-乙二胺光度法测定;TN采用过硫酸钾氧化紫外分光光度法测定。本研究中所有水质指标的测定,均取3次平行样进行测试,取平均值作图与描述规律。2)反应动力学方法。本研究探讨的反应动力学基于硝化反应和反硝化反应的Monod方程[10]。对于硝化反应,其限制因素为
$ {\rm{NH}}_4^ + $ -N浓度和DO,因此,硝化反应的Monod方程如式(1)所示。式中:v硝化为硝化反应比硝化速率,mg·(g·h)−1;v硝化,max为最大比硝化速率,mg·(g·h)−1;SN为
$ {\rm{NH}}_4^ + $ -N的底物浓度,mg·L−1;kSN为$ {\rm{NH}}_4^ + $ -N的饱和常数,mg·L−1;SO为DO的底物浓度,mg·L−1;kSO为DO的饱和常数,mg·L−1。在本研究中,为了保证好氧池的硝化过程完全进行,且本研究不探究低温低C/N条件下DO的影响,所以在曝气池中给予过量的曝气,可以认为SO>>kSO,所以SO/(kSO+SO)≈1。因此,本研究探究的硝化反应动力学Monod方程如式(2)所示。
同理,由于反硝化反应中的限制因素为
${\rm{NO}}_3^ - $ -N浓度和碳源浓度,所以反硝化反应动力学Monod方程如式(3)所示。式中:v反硝化为反硝化反应比反硝化速率,mg·(g·h)−1;v反硝化,max为最大比反硝化速率,mg·(g·h)−1;S'N为
${\rm{NO}}_3^ - $ -N的底物浓度,mg·L−1;k'SN为${\rm{NO}}_3^ - $ -N的饱和常数,mg·L−1;SC为碳源的底物浓度,mg·L−1;kSC为碳源的饱和常数,mg·L−1。硝化反应动力学:补充人工配水并搅拌均匀后,开始曝气并立即取样,而后每30 min取样1次,测定水样的
$ {\rm{NH}}_4^ + $ -N浓度,绘制$ {\rm{NH}}_4^ + $ -N浓度随时间变化的曲线,并且计算每一段时间间隔内的比硝化速率(即每一段曲线的斜率除以污泥浓度)。以$ {\rm{NH}}_4^ + $ -N浓度为横坐标,以比硝化速率为纵坐标,绘制Monod曲线并进行拟合,得到v硝化,max和kSN的拟合值。反硝化反应动力学:探究
${\rm{NO}}_3^ - $ -N底物作为限制因素时,在体系中添加过量的碳源,即SC>>kSC,使SC/(kSC+SC)≈1,通过v反硝化=v反硝化,max·S'N/(k'SN+S'N)拟合得到v反硝化,max和k'SN;探究碳源底物浓度作为限制因素时,在体系中添加过量的${\rm{NO}}_3^ - $ -N,即S'N>>k'SN,使S'N/(k'SN+S'N)≈1,通过v反硝化=v'反硝化,max·SC/ (kSC+SC)拟合得到v'反硝化,max和kSC。理论上v反硝化,max与v'反硝化,max相同或相近。综合以上结果,利用动力学参数v反硝化,max、k'SN和kSC,得到反硝化反应的Monod方程。
1.1. 活性污泥接种与驯化
1.2. 实验装置与运行参数
1.3. 分析方法
-
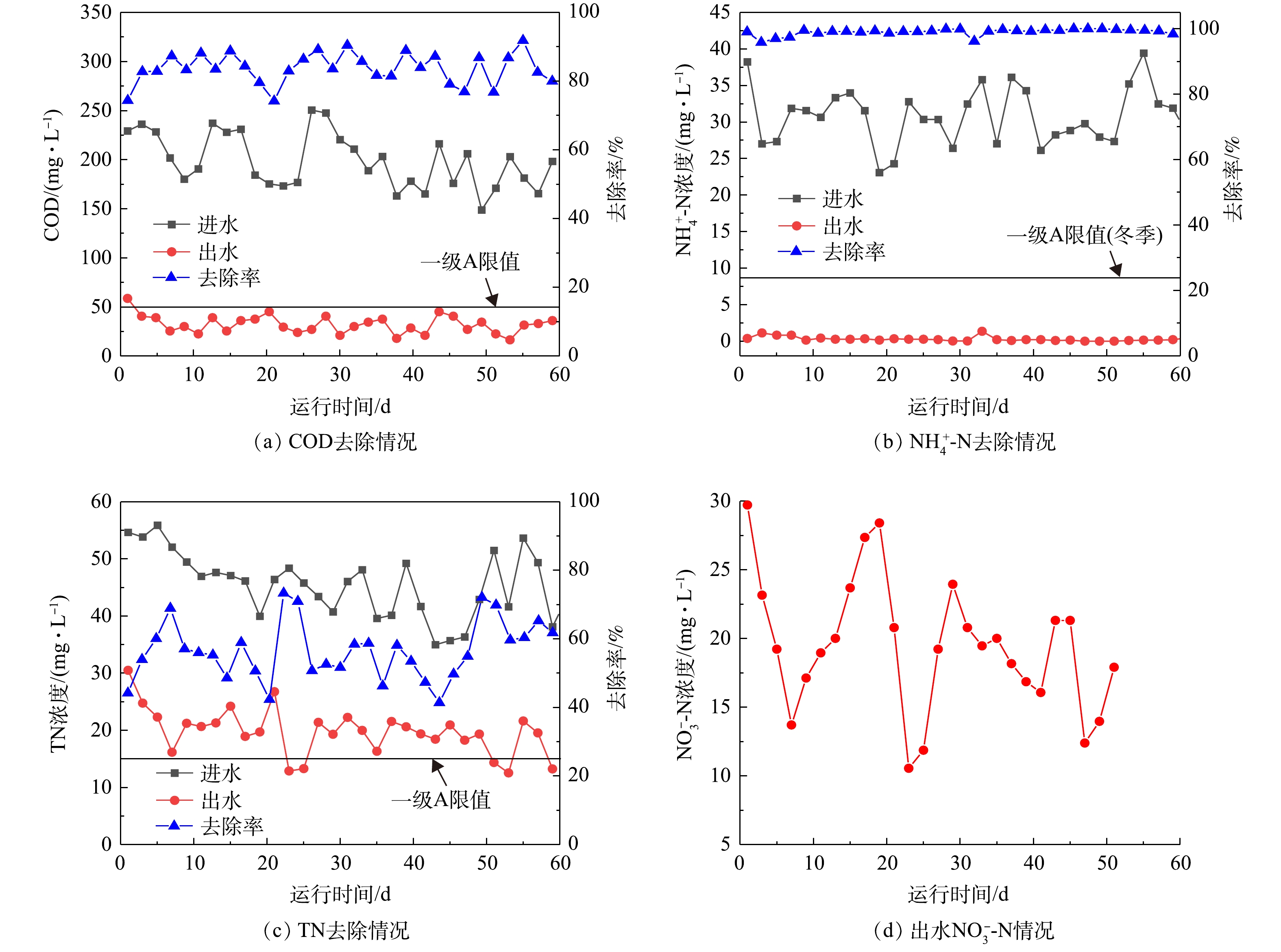
低温低C/N进水条件下,连续运行A2/O中试装置约60 d,其进出水情况及主要污染物的去除特性见图2。
1) COD去除情况。在实验期间,进水COD均保持在150~250 mg·L−1,平均浓度为198.95 mg·L−1,出水的情况如图2(a)所示。其数值基本均达到了《城镇污水处理厂污染物排放标准(GB 18918-2002)》一级A的排放标准(COD<50 mg·L−1),平均浓度为32.27 mg·L−1。但是,从去除率的角度上看,当进水COD较低时,A2/O系统的COD去除率偏低,一般为80%~85%,有时甚至低于80%,平均去除率为83.7%,这表明整个系统对COD去除的潜力还未被完全开发。结果表明,当进水COD偏低时,活性污泥微生物可用来进行生长繁殖的物质较少,以及低温时微生物的活性受到抑制,所以,在持续低COD进水的条件下,活性污泥的增长速率低于常规工况,当排泥没有进行相应的调整时,整个系统的MLSS逐渐下降到较低的水平。随着系统的微生物量降低,可以被微生物生化反应去除的有机物相应减少,导致系统的COD去除率偏低。但是,由于实验中进水COD较低,所以出水仍能达到一级A的排放标准。
2)
$ {\rm{NH}}_4^ + $ -N去除情况。实验期间$ {\rm{NH}}_4^ + $ -N的进出水情况如图2(b)所示。$ {\rm{NH}}_4^ + $ -N的进水浓度为30~40 mg·L−1,出水$ {\rm{NH}}_4^ + $ -N基本为0 mg·L−1,平均去除率为99.0%,且不随进水$ {\rm{NH}}_4^ + $ -N浓度的波动而产生变化,这说明低温低C/N的进水条件对硝化过程影响较小。初步分析可认为,由于硝化细菌AOB和NOB为自养型微生物,进水低C/N并不影响其生长繁殖,反而由于异养型微生物的生长繁殖受到限制,在溶解氧的竞争方面,硝化细菌成为优势菌群;另一方面,运行过程中曝气池的DO不低于2.5 mg·L−1,完全满足硝化反应的需要[12]。因此,尽管硝化过程对低温高度敏感[13],但硝化细菌占优势、曝气池DO高,所以,从整体上来看,$ {\rm{NH}}_4^ + $ -N的去除未受到较大影响。3) TN去除情况。实验期间TN的进出水情况如图2(c)所示。实验期间进水TN为40~50 mg·L−1,属于一般城镇污水处理厂进水的典型值。而进水的C/N较低,COD/TN的平均值为4.43,存在碳源不足的情况。因此,从出水来看,该条件下A2/O系统对TN的去除效果较差。在部分时间段内,出水TN能够达到《城镇污水处理厂污染物排放标准》(GB 18918-2002)一级A的排放标准(TN<15 mg·L−1),实验期间的出水TN基本在20 mg·L−1左右,甚至出现超过30 mg·L−1的情况。去除率根据经验公式(式(4))计算。
在外回流r为100%,内回流R为250%的运行工况下,TN去除率的理论值应为77.8%,但实验结果表明,低温低C/N条件下TN的去除率仅为50%~73%,平均去除率为56.5%,明显偏低。结合前文对
$ {\rm{NH}}_4^ + $ -N去除的分析,可以认为,出水TN偏高、去除率偏低的原因在于${\rm{NO}}_3^ - $ -N和${\rm{NO}}_2^ - $ -N的去除效果不好,即反硝化效果较差。由图2(d)可见,出水中的${\rm{NO}}_3^ - $ -N浓度与出水TN浓度相近,变化趋势相同,这证实了反硝化效果差的推测。初步分析可认为,导致反硝化效果差的原因有以下3点:一是由于反硝化菌属于异养型微生物,在低C/N进水时,碳源不足导致反硝化菌进行生化反应受到限制;二是低温条件下与反硝化反应相关的酶活性受到严重抑制,反硝化反应的速率明显下降[14];三是低温导致DO过度饱和,内回流将大量DO带入缺氧池,破坏缺氧环境,对反硝化过程造成不利影响[15]。在本研究中,缺氧池的DO为0.61 mg·L−1,ORP为93 mV,一般缺氧池DO为0.2~0.3 mg·L−1,ORP为−100~+100 mV,这证明了内回流DO过高引起破坏缺氧环境的结论。 -
沿程实验是在A2/O中试装置的进水口、厌氧池出口、缺氧池出口、好氧池出口和二沉池出口(图1(a)中的①~⑤)分别取样,测定水质指标,并通过水质指标的变化规律来评价系统各段生化反应的效果。水质测试结果见表2。
在
${\rm{NO}}_2^ - $ -N方面,通过沿程实验可以看到,整个系统中${\rm{NO}}_2^ - $ -N浓度均较低,没有出现${\rm{NO}}_2^ - $ -N的积累,其对于出水TN的影响不大,因此,不对${\rm{NO}}_2^ - $ -N进行详细描述与分析。1) COD的沿程转化规律。进水COD为204.80 mg·L−1,在外回流r为100%的工况下,进入厌氧池的COD应当为113.95 mg·L−1左右,而厌氧池的出水COD为62.67 mg·L−1,这表明有45.0%的COD在厌氧阶段被消耗,其主要生化过程是聚磷菌的厌氧释磷。在内回流比R为250%时,进入缺氧池的COD应当为42.06 mg·L−1左右,而缺氧池的出水COD为28.59 mg·L−1,即有32.0%的COD在缺氧阶段被消耗,其主要生化过程是反硝化反应。最后,污水经过好氧池和二沉池,COD均有少量下降,主要是少量的异养型微生物进行有机物的利用。但是,由于COD已经处于较低的水平,异养型微生物相比于自养型微生物——硝化细菌的竞争优势弱,因此,这部分异养型微生物的量较少,对COD去除的效果不明显。
2)
${\rm{NO}}_3^ - $ -N的沿程转化规律。在R为250%的工况下,进入缺氧池的${\rm{NO}}_3^ - $ -N浓度应当为11.78 mg·L−1左右,而缺氧池出口的${\rm{NO}}_3^ - $ -N浓度为9.18 mg·L−1,故仅有22%左右的${\rm{NO}}_3^ - $ -N被还原为N2,没有达到反硝化的要求。理论计算表明,还原1 g·L−1${\rm{NO}}_3^ - $ -N被还原为N2需要的COD为2.86 g·L−1,该沿程实验中缺氧池总共消耗的COD为13.47 mg·L−1,理论上还原的${\rm{NO}}_3^ - $ -N为4.71 mg·L−1,但实际还原的${\rm{NO}}_3^ - $ -N仅为2.60 mg·L−1,为理论值的55%。这说明有45%左右的碳源被反硝化细菌用于自身生长繁殖或被反硝化细菌以外的其他微生物利用了,而不是用于反硝化反应。导致这种情况的原因是:一方面,低温导致缺氧池DO偏高(表2),使得其他兼性异养微生物处于优势地位,反硝化细菌可用于生长繁殖和反硝化反应的碳源被竞争者大量侵占,进而影响反硝化效果;另一方面,反硝化细菌在低温、高DO环境下活性受到抑制,使得反硝化反应的速率大大降低,所以,在与常规工况相同的缺氧池水力停留时间(HRT)里,能被反硝化反应还原的${\rm{NO}}_3^ - $ -N减少。以上两方面的原因导致出水中${\rm{NO}}_3^ - $ -N的浓度偏高、TN不达标。3)
$ {\rm{NH}}_4^ + $ -N的沿程转化规律。在r为100%、R为250%的工况下,厌氧池、缺氧池进水的$ {\rm{NH}}_4^ + $ -N浓度应当分别为12.96 mg·L−1和6.49 mg·L−1,该数值与厌氧池、缺氧池的出水$ {\rm{NH}}_4^ + $ -N浓度接近,符合这2个阶段不发生硝化反应的常识。在好氧池,$ {\rm{NH}}_4^ + $ -N由6.14 mg·L−1降低到2.08 mg·L−1,再到二沉池出水降低为1.02 mg·L−1,完全达到了一级A(冬季,$ {\rm{NH}}_4^ + $ -N<8 mg·L−1)的标准。由此可见,低温低C/N条件下,A2/O系统的硝化过程没有受到太大影响。 -
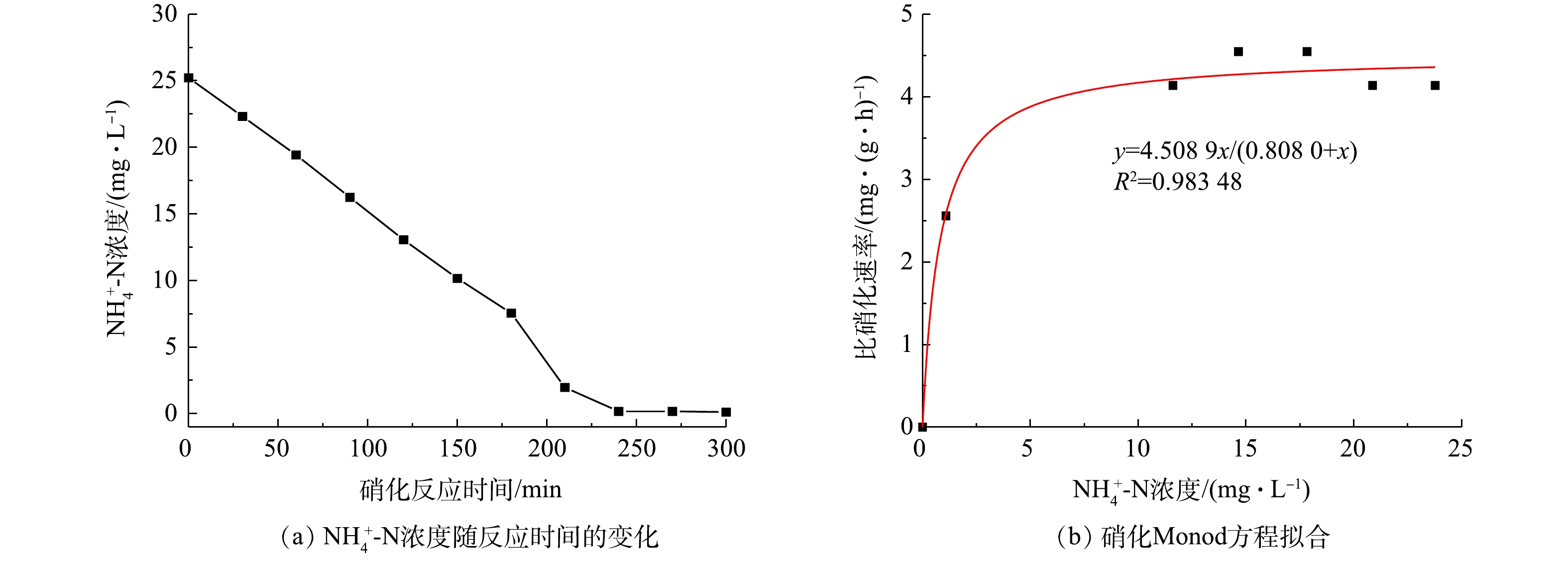
硝化反应Monod方程的实验结果和拟合结果如图3所示。图3(a)显示,当体系中
$ {\rm{NH}}_4^ + $ -N浓度较高时,硝化反应近似为零级反应,比硝化速率达到最大且不随$ {\rm{NH}}_4^ + $ -N浓度的降低而降低,$ {\rm{NH}}_4^ + $ -N浓度随时间变化的曲线近似为直线;但当$ {\rm{NH}}_4^ + $ -N浓度降低到5 mg·L−1附近时,硝化反应速率开始急剧下降。用各段时间间隔内的比硝化速率与$ {\rm{NH}}_4^ + $ -N浓度进行拟合(图3(b)),得到低温条件下的硝化Monod方程,如式(5)所示。式中:v硝化,max为4.508 9 mg·(g·h)−1,即最大硝化速率为4.508 9 mg·(g·h)−1;kSN为0.808 0 mg·L−1,即当
$ {\rm{NH}}_4^ + $ -N浓度降低为0.808 0 mg·L−1时,硝化反应速率为峰值的50%。DINÇER等[11]的研究表明,在20 ℃下,v硝化,max为47.92 mg·(g·h)−1,kSN为5.14 mg·L−1。本研究中得到的值明显低于此值。这说明,在低温的条件下,硝化反应受到严重影响,导致最大硝化速率大幅降低,而饱和常数较低表明此条件下的硝化反应以较为稳定的反应速率进行,速率骤降点延后。这一现象的原因可能是:低温低C/N条件驯化的活性污泥对体系中
$ {\rm{NH}}_4^ + $ -N浓度的变化不敏感,只有当$ {\rm{NH}}_4^ + $ -N浓度降低到足够低的水平时,比硝化速率才出现突变。结合A2/O中试实验的情况分析,低温低C/N进水中,$ {\rm{NH}}_4^ + $ -N的浓度与常规工况并无明显差异,因此,活性污泥对$ {\rm{NH}}_4^ + $ -N浓度的适应性没有发生明显变化,表现为比硝化速率对$ {\rm{NH}}_4^ + $ -N浓度的变化不敏感。低温低C/N进水条件对硝化过程的影响主要体现在最大比硝化速率的降低。 -
1)
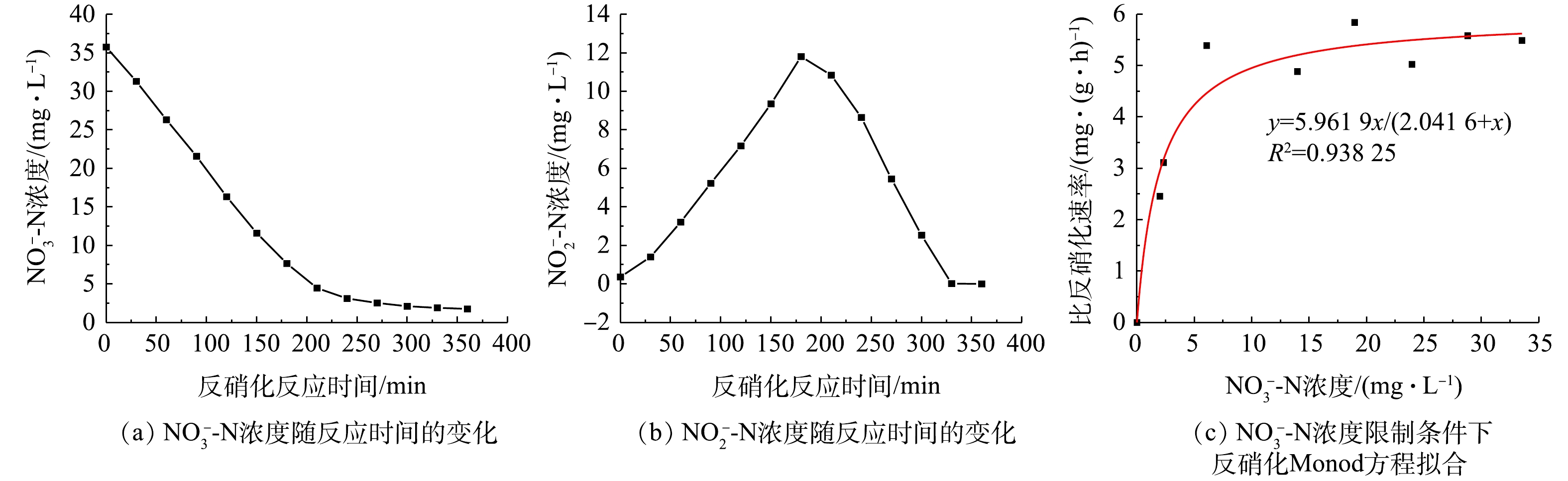
${\rm{NO}}_3^ - $ -N浓度限制条件下反硝化Monod方程拟合。在计算比反硝化速率时,被还原的硝氮浓度为Δ${\rm{NO}}_3^ - $ -N–0.6Δ${\rm{NO}}_2^ - $ -N,该式表示实际被还原的${\rm{NO}}_3^ - $ -N的量[16]。${\rm{NO}}_3^ - $ -N的沿时变化情况如图4(a)所示。当${\rm{NO}}_3^ - $ -N浓度在10 mg·L−1以上时,反硝化反应为零级反应,比反硝化速率不会随着${\rm{NO}}_3^ - $ -N浓度的降低而减小,此时的曲线近似为一条直线。当${\rm{NO}}_3^ - $ -N浓度在5 mg·L−1左右时,反硝化速率开始受到${\rm{NO}}_3^ - $ -N浓度过低的限制,速率开始急剧下降,曲线变缓。${\rm{NO}}_2^ - $ -N的沿时变化情况如图4(b)所示。如前文所述,在反硝化过程中,${\rm{NO}}_3^ - $ -N并非直接还原为N2,而是有中间过程:${\rm{NO}}_3^ - $ -N先还原为${\rm{NO}}_2^ - $ -N,${\rm{NO}}_2^ - $ -N再还原为N2,其中,后者为限速步骤。因此,在反硝化过程中会出现${\rm{NO}}_2^ - $ -N的积累,${\rm{NO}}_2^ - $ -N浓度的最大积累量达到11.81 mg·L−1。在
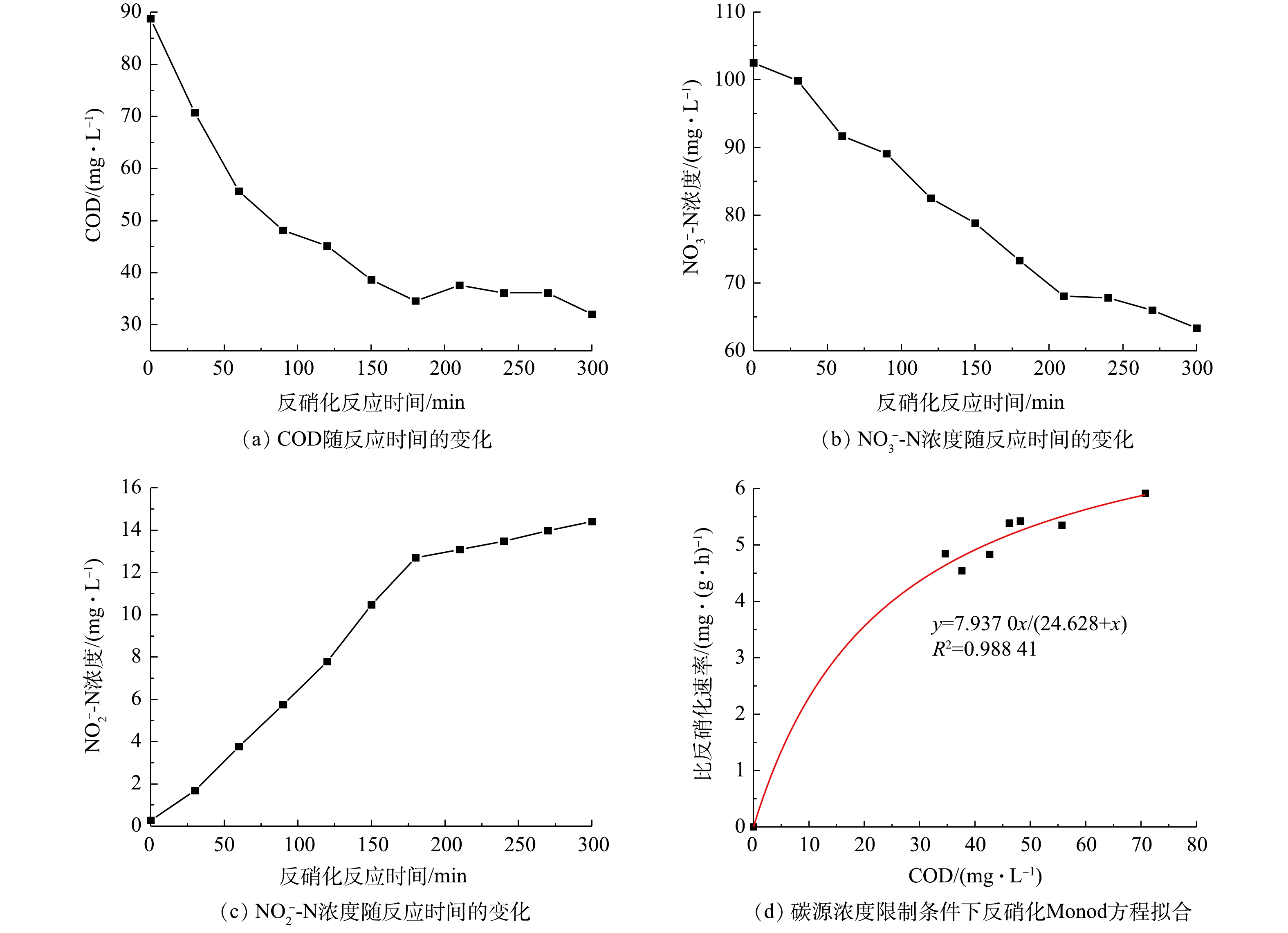
${\rm{NO}}_3^ - $ -N浓度限制条件下,反硝化Monod方程的拟合如图4(c)所示。动力学参数v反硝化,max为5.961 9 mg·(g·h)−1,表示实验条件下最大反硝化速率为5.961 9 mg·(g·h)−1;k'SN为2.041 6 mg·L−1,表示当${\rm{NO}}_3^ - $ -N浓度降低为2.041 6 mg·L−1时,比反硝化反应速率降低为峰值的50%;R2为0.938 25。2)碳源限制条件下反硝化Monod方程拟合。如图5所示,在碳源浓度成为限制因素时,
${\rm{NO}}_3^ - $ -N浓度和${\rm{NO}}_2^ - $ -N浓度的降低都明显有2个阶段:第1阶段碳源的量还充足,反硝化反应可以以最大速率进行;第2阶段碳源明显不足,${\rm{NO}}_3^ - $ -N浓度和${\rm{NO}}_2^ - $ -N浓度降低的趋势放缓。这个结果与马勇等[17]的研究结果一致。结合COD的沿时变化(图5(a))对原因进行分析,可以看到,当COD降低为50 mg·L−1左右时,COD降低的趋势开始变缓,并在36 mg·L−1左右不再下降。在这个过程中,由于反硝化细菌可利用的碳源越来越少,导致反硝化速率呈现逐渐降低的趋势。碳源浓度为限制因素时的反硝化Monod方程拟合情况如图5(d)所示。动力学参数v'反硝化,max为7.937 0 mg·(g·h)−1,表示实验条件下最大反硝化速率为7.937 0 mg·(g·h)−1,与v反硝化,max有较大差距。其原因在于:Monod方程探究实验中,水温、氧化还原电位(ORP)等参数不好控制,多组实验时条件存在差异,所以拟合出来的结果有差别。为方便得到最后的反硝化Monod方程,这里把v反硝化,max和v'反硝化,max的平均值作为最大反硝化速率v''反硝化,max,其值为6.949 5 mg·(g·h)−1;kSC为24.628 mg·L−1,表示当COD为24.628 mg·L−1时,比反硝化反应速率降低为峰值的一半;R2为0.988 41,方程的拟合度较高。
综上所述,低温低C/N条件下反硝化反应的Monod方程为如式(6)所示。
DINÇER等[11]的研究表明,在20 ℃下,v反硝化,max为9.58 mg·(g·h)−1,k'SN为0.27 mg·L−1,kSC为60 mg·L−1。本研究中得到的v反硝化,max和kSC均低于前述值,仅k'SN的值偏高。这说明,在低温低C/N的条件下,反硝化反应受到一定的影响,导致最大反应速率亦在一定程度上降低。而
${\rm{NO}}_3^ - $ -N饱和常数较高、COD饱和常数较低,表明低温C/N条件下,比反硝化速率对COD的变化不敏感,对${\rm{NO}}_3^ - $ -N浓度的变化敏感。与常规工况相比,在相同的${\rm{NO}}_3^ - $ -N浓度下,低温低C/N进水条件下驯化的活性污泥的比反硝化速率较低。尽管比反硝化速率对COD的变化不敏感,但进水COD较常规工况低也会直接导致比反硝化速率的小幅度降低。该反硝化动力学模型可以在理论上指导污水处理厂高效投加碳源。污水处理厂缺氧池的HRT通常是确定的,对于确定的脱氮目标(即需要通过反硝化脱氮的量)而言,目标反硝化速率是确定的。根据该反硝化动力学模型,能推算出缺氧池需要保持的COD水平,再根据该值与缺氧池进水COD的差值,即可确定碳源投加的理论量,从而可在一定程度上避免盲目投加碳源所造成的浪费。
2.1. 污染物去除特性
2.2. COD与氮素沿程转化规律
2.3. 硝化反应动力学
2.4. 反硝化反应动力学
-
1) A2/O中试装置在低温低C/N条件下运行的结果表明,其对COD的去除可以达到一级A排放标准,但潜力没有完全发挥;对氨氮可以基本去除,去除率达99.0%;对
${\rm{NO}}_3^ - $ -N、TN的去除不理想,对TN的平均去除率仅为56.5%。2)碳源不足是导致反硝化效果差的重要原因。低C/N进水导致缺氧池碳源缺乏,在此基础上只有45%的碳源用于反硝化反应,剩余碳源被其他异养型微生物竞争,导致出水TN超标。
3)在低温和低C/N条件下,v硝化,max、v反硝化,max均比常规状态下低,这说明低温低C/N进水条件严重影响硝化和反硝化反应的速率;
$ {\rm{NH}}_4^ + $ -N、COD的饱和常数比常规状态下高,${\rm{NO}}_3^ - $ -N的饱和常数比常规状态下低,表明低温低C/N进水条件下,硝化反应对$ {\rm{NH}}_4^ + $ -N浓度的变化不敏感,反硝化反应对COD的变化不敏感、对${\rm{NO}}_3^ - $ -N浓度的变化敏感。







 下载:
下载: