N,N’-取代对苯二胺(PPD)是橡胶中广泛使用的抗氧化剂[1],人们将常见的对苯二胺类抗氧化剂统一称为PPDs。据估计,全球每年生产近31亿条轮胎[2],对PPDs有较高的需求。仅在中国,2009年PPDs消耗量超过10万t [3]。N-异丙基-N’-苯基-1,4-苯二胺(IPPD)、N-苯基-N’-环己基对苯二胺(CPPD)、N,N’-二苯基对苯二胺(DPPD)、N-(1,3-二甲基丁基)-N’-苯基对苯二胺(6PPD)、N,N’-二-2-萘基对苯二胺(DNPD)和N,N’-(1,4-二甲基戊基)-对苯二胺(77PD)是常见的对苯二胺类抗氧化剂[4]。其中,6PPD对淡水生物具有急性和慢性毒性[5],并可能引起人类皮肤过敏反应。IPPD对人胚胎肺成纤维细胞有一定的毒性[6]。DPPD对大鼠具有生殖和发育毒性[7]。近年来,人们发现6PPD的臭氧转化产物,6PPD-quinone (6PPD-Q)对银大马哈鱼(coho salmon)具有急性致死效应(半数致死浓度LC50 < 95 ng·L-1)。进而开始关注PPDs及其衍生物的环境水平和健康风险。橡胶制品的广泛使用导致PPDs及其衍生物大量释放到环境中。PPDs作为抗氧化剂应用于橡胶产品,特别是用于生产轮胎、管道、皮带和鞋底的橡胶材料[8],还可能被应用于制备染发剂[9]、指甲油染料[10]、润滑剂[11]等。越来越多的研究表明PPDs和6PPD-Q在尘土[8,12-15]、大气颗粒物[16-18]、地表径流[19-22]、沉积物[23-24]、食品[25]以及人类尿液[26]中广泛存在。
道路尘土是PPDs和6PPD-Q主要的赋存介质,可以直接随着雨水进入地表径流进而对水生生物带来危害,因此全面开展PPDs和6PPD-Q在道路尘土中的污染特征研究至关重要。目前为止,有关尘土及土壤中PPDs和6PPD-Q的数据十分有限。Huang等[8]报道了中国广州地区道路尘土中6种PPDs (ΣPPDs)的总浓度为20.3~543 ng·g-1,其中IPPD浓度为3.0~88.1 ng·g-1,77PD浓度为
为探讨PPDs和6PPD-Q的区域污染特征,以大连市为研究对象开展试验,从与居民日常生活密切相关的不同区域采集样品,包括主干道、居民区道路和居民广场的尘土样品,以及居民区绿化带、农田表层的土壤样品,采用高效液相色谱串联质谱法(HPLC-MS/MS)对样品中的6种PPDs以及6PPD-Q进行定量分析,并对比了尘土与土壤样品中目标物质的污染特征,进一步根据美国环境保护局(US EPA)的风险评估模型,估计了道路源尘土中目标化合物对儿童及成人的暴露量,以期为保护人群健康提供基础数据。
1 材料与方法(Materials and methods)
1.1 试剂与仪器
材料与试剂:PPDs抗氧化剂标准品(IPPD、DPPD、CPPD、6PPD、77PD、DNPD)和6PPD-Q分别购自阿拉丁(中国上海)、玛雅试剂(中国上海)、凯为化学(中国上海)、百灵威(中国北京)、TCI化学(日本东京)和加拿大多伦多研究化学(加拿大多伦多)。2个内标苯胺-d5和6PPD-Q-d5分别购自加拿大多伦多研究化学和上海安谱实验科技股份有限公司(中国)。试验所用试剂丙酮(农残级)购自美国Fisher公司,二氯甲烷(农残级)购自美国J.T.Baker公司,乙腈(HPLC-MS级)购自美国默克公司,超纯水由Millipore超纯水设备制备而成(Millipore, Billerica, MA, USA)。
仪器:土壤玛瑙研磨机(中国长沙米淇公司,MITR-TRXQM-1L),超声波清洗仪(美国Branson公司,B5200S),氮气吹干仪(中国北京八方世纪科技有限公司,BF2000),旋转蒸发仪(瑞士Buchi公司,Rotavapor R-205),电子天平(中国上海精密仪器仪表有限公司,JA-2003型),移液器(德国艾本德公司,Eppendorf Research® plus),Milli-Q超纯水(美国,Millipore),高效液相色谱-三重四极杆质谱联用仪(美国Thermo公司,HPLC-MS/MS,TSQ Quantum Access),台式低速离心机(中国上海力辰仪器科技有限公司,LC-LX-L40B),氮气吹扫仪(中国上海安谱实验科技股份有限公司,DC12H),凝胶渗透色谱仪(中国大连依利特分析仪器有限公司,GPC-P230)。
1.2 样品采集
2022年9月—2023年3月,在大连市共采集样品39份:其中尘土样品19份,包括城市主干道(urban trunk dust, UD; N=7)、居民区道路(residential dust, CD; N=7)以及居民广场(residential plaza dust, SQ; N=5);表层土样品20份,采集于高速公路两侧10 m范围内农田(agricultural land, FS; N=13)以及居民区绿化带(residential green belt, CS; N=7),将表面杂草等杂质去除后,采集表层土。使用预先清洗过的毛刷采集道路尘土和表层土样品,为减少交叉污染,每个采样点使用一个新的刷子,然后用铝箔纸包裹放入聚乙烯密封袋,运入实验室在-20 ℃下储存至提取和分析。采样点地理信息如表1所示。
表1 试验采样点地理信息
Table 1 Geographical information of test sampling sites
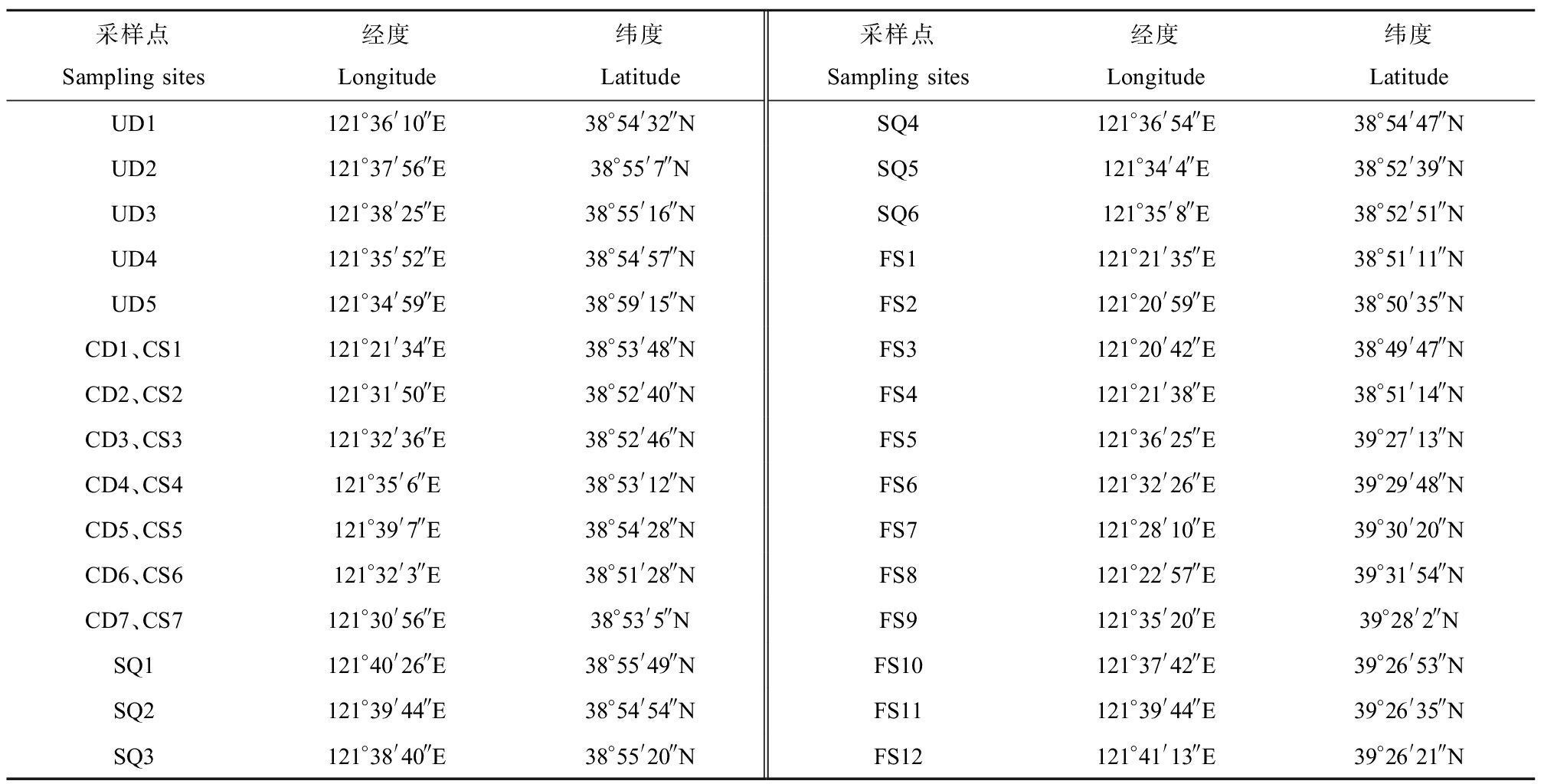
采样点Sampling sites经度Longitude纬度Latitude采样点Sampling sites经度Longitude纬度LatitudeUD1121°36'10″E38°54'32″NSQ4121°36'54″E38°54'47″NUD2121°37'56″E38°55'7″NSQ5121°34'4″E38°52'39″NUD3121°38'25″E38°55'16″NSQ6121°35'8″E38°52'51″NUD4121°35'52″E38°54'57″NFS1121°21'35″E38°51'11″NUD5121°34'59″E38°59'15″NFS2121°20'59″E38°50'35″NCD1、CS1121°21'34″E38°53'48″NFS3121°20'42″E38°49'47″NCD2、CS2121°31'50″E38°52'40″NFS4121°21'38″E38°51'14″NCD3、CS3121°32'36″E38°52'46″NFS5121°36'25″E39°27'13″NCD4、CS4121°35'6″E38°53'12″NFS6121°32'26″E39°29'48″NCD5、CS5121°39'7″E38°54'28″NFS7121°28'10″E39°30'20″NCD6、CS6121°32'3″E38°51'28″NFS8121°22'57″E39°31'54″NCD7、CS7121°30'56″E38°53'5″NFS9121°35'20″E39°28'2″NSQ1121°40'26″E38°55'49″NFS10121°37'42″E39°26'53″NSQ2121°39'44″E38°54'54″NFS11121°39'44″E39°26'35″NSQ3121°38'40″E38°55'20″NFS12121°41'13″E39°26'21″N
注:UD表示城市主干道尘土,CD表示居民区道路尘土,SQ表示居民广场尘土;FS表示高速公路两侧10 m范围内农田表层土,CS表示居民区绿化带表层土。
Note: UD indicates urban trunk road dust, CD indicates residential road dust, SQ indicates residential square dust; FS indicates farmland topsoil within 10 m on both sides of the highway, and CS indicates residential green belt topsoil.
1.3 样品前处理
尘土与土壤样品去除石块、树枝等杂质后自然风干,然后用球磨机磨碎至完全通过150 μm孔径铜质标准筛。取0.5 g样品放入15 mL玻璃离心管内,加入20 ng提取内标(6PPD-Q-d5),10 mL丙酮,超声15 min×3次,合并提取液并在3 000 r·min-1离心力下离心5 min,上清液转移至100 mL平底烧瓶中。经旋转蒸发后氮吹浓缩至近干,加入2 mL二氯甲烷复溶,将溶液通过0.22 μm PTFE滤膜后通过GPC进一步去除提取液中的脂质,GPC流动相为二氯甲烷,检测器波长为254 nm,设置流速为5 mL·min-1,收集22~38 min的流出组分,旋转蒸发后氮吹浓缩至近干,加入20 ng进样内标苯胺-d5,用乙腈定容至1 mL,过0.22 μm PTFE滤膜后储存至棕色液相小瓶中待上机分析。
1.4 仪器分析
采用HPLC-MS/MS对目标化合物进行定量分析。液相参数:色谱分离采用C8液相色谱柱(100 mm × 2.1 mm,1.7 μm,ACQUITY UPLC,美国Waters)。流动相A为含0.8%(m∶m)乙酸铵的水(pH=3),流动相B为乙腈,流速为0.18 mL·min-1。流动相梯度为:0~20 min:40%B~92%B;20~20.2 min:92%B~100%B;20.2~30 min:100%B~40%B。进样量为10 μL,色谱柱温度设定为25 ℃。
质谱参数:电喷雾离子源,正离子电离模式(ESI+);电离电压:3.5 kV;辅助气压力:7.0×104 Pa;鞘气压力:2.8×105 Pa,传输毛细管温度为300 ℃,鞘气温度为340 ℃,碰撞气压力为0.2 Pa。采集数据模式:多反应监测(MRM)。7种目标物质的质谱参数如表2所示。
表2 目标化合物的HPLC-MS/MS参数
Table 2 HPLC-MS/MS parameters of target compounds
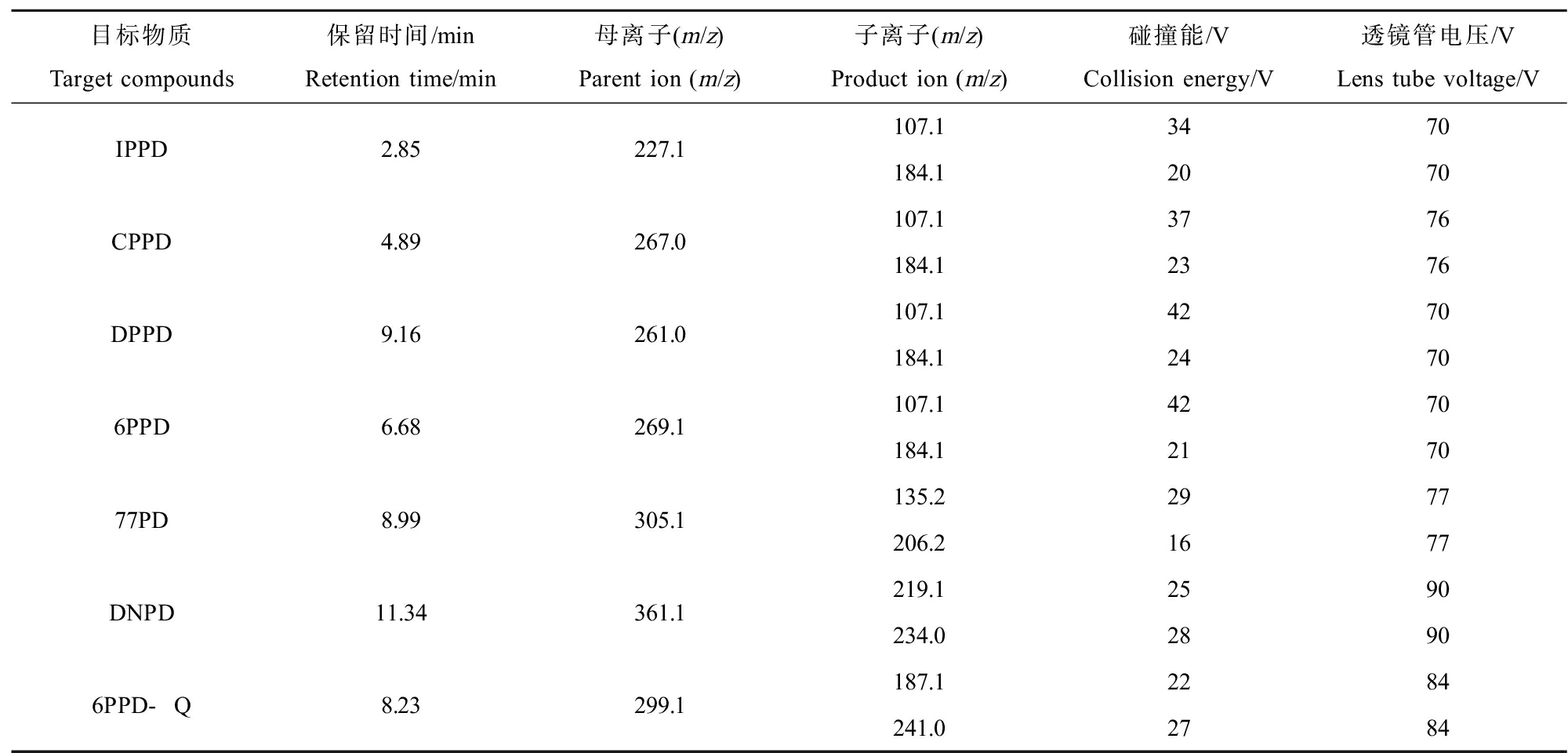
目标物质Target compounds保留时间/minRetention time/min母离子(m/z)Parent ion (m/z)子离子(m/z)Product ion (m/z)碰撞能/VCollision energy/V透镜管电压/VLens tube voltage/VIPPD2.85227.1107.13470184.12070CPPD4.89267.0107.13776184.12376DPPD9.16261.0107.14270184.124706PPD6.68269.1107.14270184.1217077PD8.99305.1135.22977206.21677DNPD11.34361.1219.12590234.028906PPD-Q8.23299.1187.12284241.02784
注:IPPD表示N-异丙基-N’-苯基-1,4-苯二胺,77PD表示N,N’-(1,4-二甲基戊基)-对苯二胺,DPPD表示N,N’-二苯基对苯二胺;DNPD表示N,N’-二-2-萘基对苯二胺,6PPD表示N-(1,3-二甲基丁基)-N’-苯基对苯二胺,6PPD-Q表示6PPD-quinone,ΣPPDs表示6种PPDs总和。
Note: IPPD indicates N-isopropyl-N’-phenyl-1,4-phenylenediamine, 77PD indicates N,N’-(1,4-dimethylpentyl)-p-phenylenediamine, DPPD indicates N,N’-diphenyl-p-phenylenediamine, DNPD indicates N,N’-di-2-naphthyl-p-phenylenediamine, 6PPD indicates N-(1,3-dimethylbutyl)-N’-phenyl-p-phenylenediamine , 6PPD-Q indicates 6PPD-quinone, and ΣPPDs indicates the sum of the six PPDs.
1.5 质量保证和质量控制
为保证样品测定的准确性与可靠性,开展了一系列质控实验。目标污染物采用内标法定量分析,混合标准溶液浓度梯度为0.5~200 ng·mL-1,进样内标在标准溶液中的浓度为20 ng·mL-1,其线性回归系数R2≥0.99。为评估实验室分析过程中的潜在污染,本研究分析了3个全程空白样品(仅添加溶剂与内标),采用与样品完全相同的方法进行前处理和仪器分析,包括:丙酮超声提取3次,氮吹浓缩,二氯甲烷复溶,GPC脱脂,氮吹浓缩,复溶于乙腈中过滤并进行上机分析。在空白样品中均未检出目标物质。将6个混合样品中加入100 μL混合标准溶液
(10 ng·mL-1),采用与样品完全相同的方法进行前处理和仪器分析,得出目标化合物的方法检出限(method detection limit, MDL)为IPPD:1.47 ng·g-1、CPPD:2.29 ng·g-1、77PD:0.34 ng·g-1、DPPD:1.46 ng·g-1、DNPD:1.23 ng·g-1、6PPD:0.43 ng·g-1、6PPD-Q:0.24 ng·g-1。加标回收率实验则是将6个混合尘土样品中加入100 μL混合标准溶液(100 ng·mL-1),采用与样品完全相同的方法进行前处理和仪器分析。6种目标物质的回收率为82.87%~100.57%。6种PPDs总和(ΣPPDs)和6PPD-Q基质效应(ME)参考文献报道的方法进行评估[12, 29];使用混合尘土样品采用与样品相同的前处理方法进行提取与净化,将最终提取液溶解在1 mL乙腈中,然后取出2个相同体积(0.2 mL)的子样品。子样品A加入0.2 mL混合标准溶液,子样品B中加入0.2 mL乙腈,外标S为0.2 mL混合标准溶液+0.2 mL乙腈。ME值的计算方法是:
式中:Ai、Bi和Si分别为子样品A和B以及外标溶液中被分析物(i)的色谱峰面积。在6次测量中,7个目标分析物的基质效应值在88.29%到108.13%之间,表明基质效应较低。因此,本试验在后续的数据分析中忽略了尘土基质对6种PPDs和6PPD-Q分析的基质效应干扰。
1.6 人体暴露评估
不同环境介质中的PPDs及6PPD-Q会通过不同的暴露途径进入人体并带来健康风险。尘土中的PPDs及6PPD-Q可以通过经口摄入和皮肤接触这2种途径进入人体。因此,本研究在暴露评估中计算了成人与儿童的日摄入量,计算公式如下:
式中:DIder和DIing表示通过尘土经皮肤吸收和经口摄入途径的每日摄入量;CRS代表尘土中ΣPPDs的总浓度以及6PPD-Q的浓度(ng·kg-1);IRing代表尘土的摄入率(mg·d-1);EF代表暴露频率(d·a-1);ED代表暴露持续时间(a);BW代表体质量(kg);AT代表平均暴露时间(d);CF代表转换因子(10-6 kg·mg-1);SA代表可接触皮肤表面积(cm2);AF代表尘土对毛皮的附着系数(mg·cm-2);ABS代表吸收系数(量纲为1)。用于评估儿童和成人日摄入量的参数如表3所示,符合美国国家环境保护局风险评估指南和相关研究[27, 30-31]。
表3 评估儿童及成人暴露于PPDs和6PPD-Q的日摄入量参数
Table 3 Parameters used to estimate human exposure to PPDs and 6PPD-Q
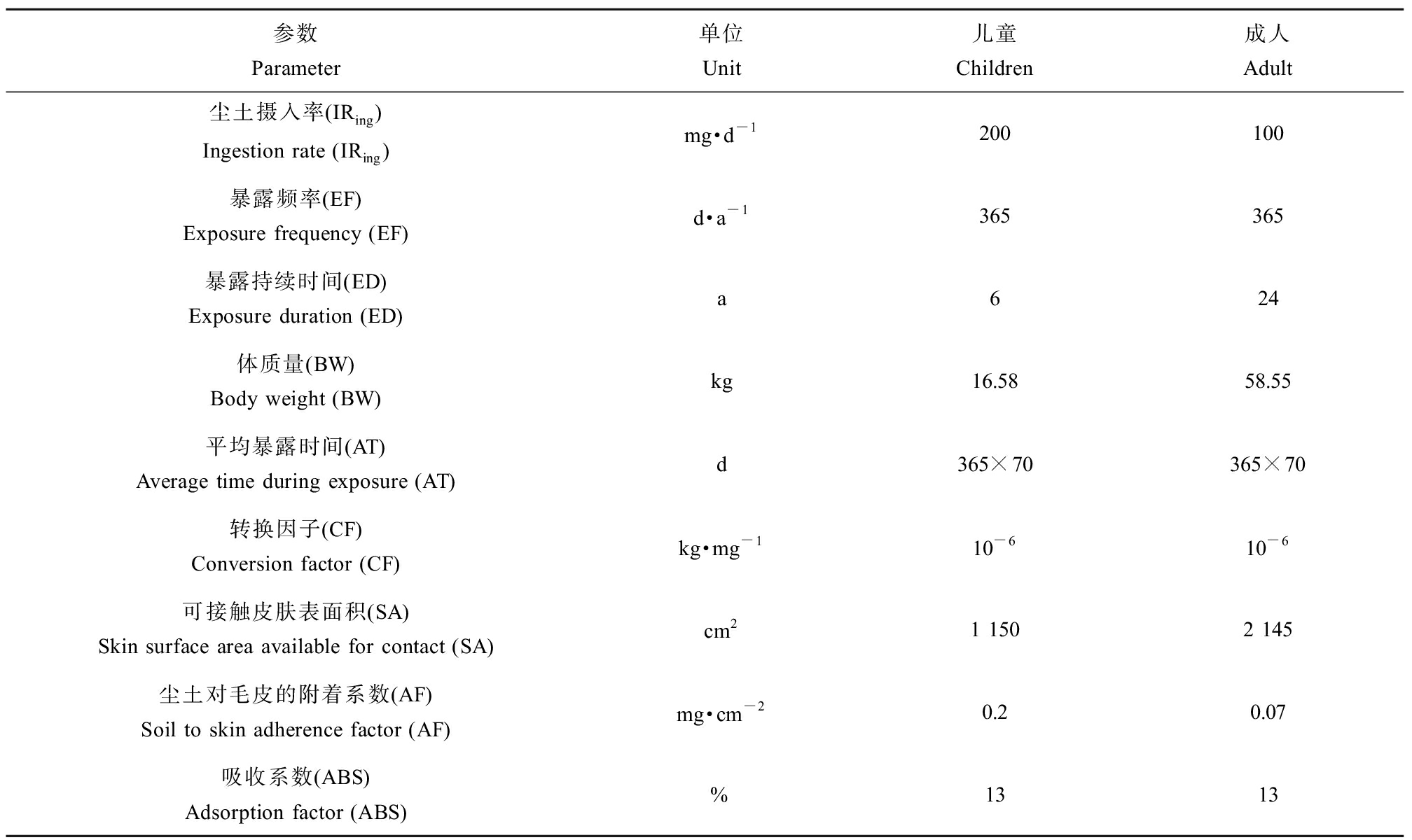
参数Parameter单位Unit儿童Children成人Adult尘土摄入率(IRing)Ingestion rate (IRing)mg·d-1200100暴露频率(EF)Exposure frequency (EF)d·a-1365365暴露持续时间(ED)Exposure duration (ED)a624体质量(BW)Body weight (BW)kg16.5858.55平均暴露时间(AT)Average time during exposure (AT)d365×70365×70转换因子(CF)Conversion factor (CF)kg·mg-110-610-6可接触皮肤表面积(SA)Skin surface area available for contact (SA)cm21 1502 145尘土对毛皮的附着系数(AF)Soil to skin adherence factor (AF)mg·cm-20.20.07吸收系数(ABS)Adsorption factor (ABS)%1313
2 结果(Results)
2.1 道路尘土和附近表层土中PPDs和6PPD-Q的污染水平
7种目标化合物中,所有样品中均未检出CPPD,后续仅对检出的6种化合物进行统计分析。不同区域样品中ΣPPDs和6PPD-Q浓度的统计结果如图1所示,6种目标化合物总浓度为2.58~175.75 ng·g-1(中值:15.27 ng·g-1),其中ΣPPDs浓度为2.46~130.22 ng·g-1(中值:10.09 ng·g-1),6PPD-Q浓度为
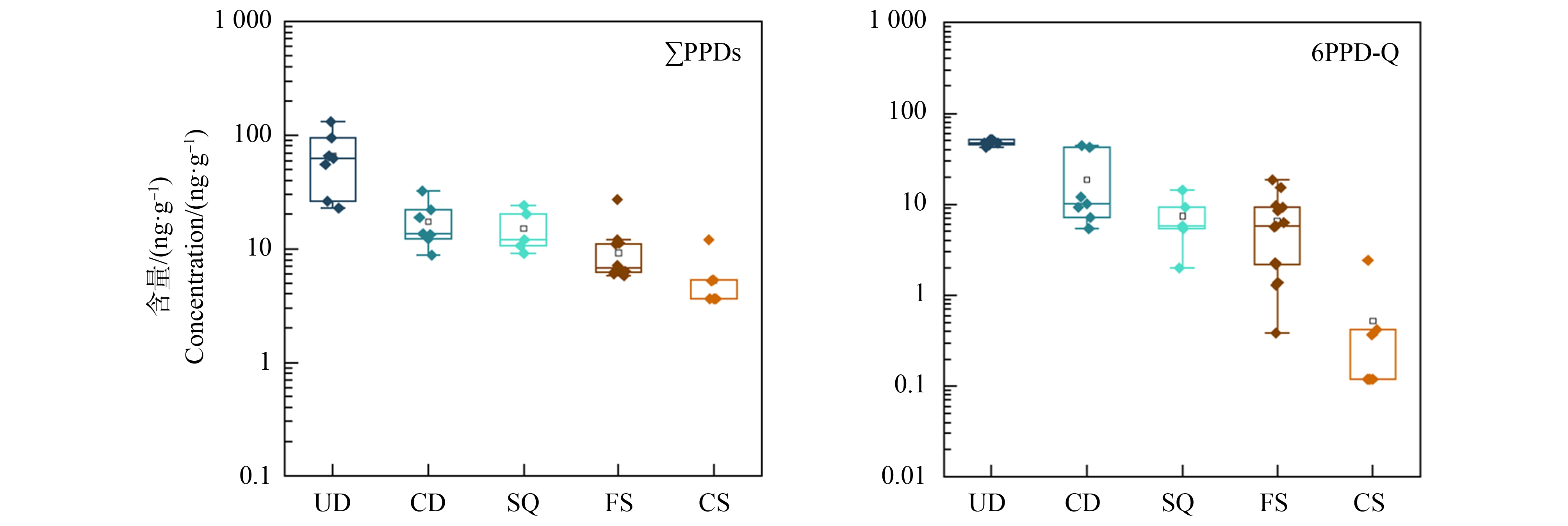
图1 道路尘土和附近表层土中ΣPPDs和6PPD-Q浓度水平
Fig. 1 Concentrations of ΣPPDs and 6PPD-Q in road dust and nearby topsoil
本研究中,道路尘土和表层土的污染水平差别较大。如图2所示,在19份尘土样品6PPD-Q、6PPD、DNPD以及77PD的检出率均为100%;而IPPD和DPPD检出率较低,均为42.10%,主干道尘土中的6PPD、DNPD和6PPD-Q浓度分别为1.61~27.26 ng·g-1 (中值:3.52 ng·g-1)、10.84~113.83 ng·g-1 (中值:19.08 ng·g-1)和42.33~52.21 ng·g-1 (中值:47.35 ng·g-1),显著高于居民区道路尘土(6PPD:0.89~3.69 ng·g-1,中值1.95 ng·g-1;DNPD:2.13~20.33 ng·g-1,中值3.78 ng·g-1;6PPD-Q:5.32~44.54 ng·g-1,中值10.07 ng·g-1) (P<0.05)和广场尘土(6PPD:1.42~1.84 ng·g-1,中值1.48 ng·g-1;DNPD:1.79~12.39 ng·g-1 ,中值3.23 ng·g-1;6PPD-Q:1.99~14.45 ng·g-1,中值5.85 ng·g-1)(P<0.05)。77PD在主干道、居民区和广场尘土中含量没有显著差异(P>0.1),浓度范围为1.65~7.57 ng·g-1。仅在主干道尘土中检测到DPPD,浓度为1.64~27.55 ng·g-1(中值:9.79 ng·g-1)。IPPD在主干道和居民区仅有一个样品检出,浓度分别为15.29 ng·g-1和2.23 ng·g-1,居民广场尘土中检出率为100%,浓度为1.52~20.33 ng·g-1。

图2 道路尘土和附近表层土中目标化合物的浓度
Fig. 2 Concentration of each target compound in road dust and nearby topsoil
农田表层土样品中77PD、6PPD和6PPD-Q的检出率均为100%,浓度范围分别为0.68~3.95 ng·g-1(中值:1.12 ng·g-1)、0.94~4.48 ng·g-1(中值:2.14 ng·g-1)和0.39~18.61 ng·g-1(中值:5.72 ng·g-1);DNPD的检出率为46.15%,浓度范围为
2.2 道路尘土和附近表层土中ΣPPDs和6PPD-Q的分布特征
不同区域样品中各目标化合物的分布特征存在差异,由于PPDs类化合物容易降解[32],而不同化合物降解速率不同,导致距离排放源较远的土壤样品中化合物的分布特征不同。在UD、CD、SQ以及FS这4个区域中,6PPD-Q是含量最高的组分,占ΣPPDs和6PPD-Q总浓度的34.54%~53.63%(平均值43.84%),其次是DNPD,占ΣPPDs和6PPD-Q总浓度的17.87%~37.06%(平均值27.48%)。由于居民区绿化带表层土(CS)中各化合物检出率较低,去掉6个化合物均未检出的CS4、CS5、CS6和CS7,其余3个样品中DNPD和77PD占比较高(图3)。主干道尘土中6PPD-Q与DNPD占ΣPPDs和6PPD-Q总浓度的79.54%;其次为DPPD和6PPD,占比分别为9.28%和6.63%;IPPD和77PD仅占总浓度的4.54%。居民区道路的6PPD-Q与DNPD占总浓度的78.42%,77PD占比为11.06%,6PPD占比为5.69%,IPPD和DPPD仅占总浓度的4.82%。居民广场中6PPD-Q与DNPD占总浓度的64.72%,77PD占比为13.63%,IPPD占比较高(9.44%),其次为6PPD(7.47%),DPPD的占比最低为4.74%。高速公路两侧农田表层土样品中各组分占比6PPD-Q(44.73%) >DNPD(17.87%) >6PPD(15.89%) >77PD(10.21%) >IPPD(6.40%) >DPPD(4.91%),77PD、DNPD和6PPD是农田表层土PPDs的主要成分,尽管三者占ΣPPDs和6PPD-Q总浓度的16.49%~70.92%,但对ΣPPDs含量的贡献在70%以上,说明这3种抗氧化剂广泛应用于橡胶及其相关制品的制造中[33-35]。
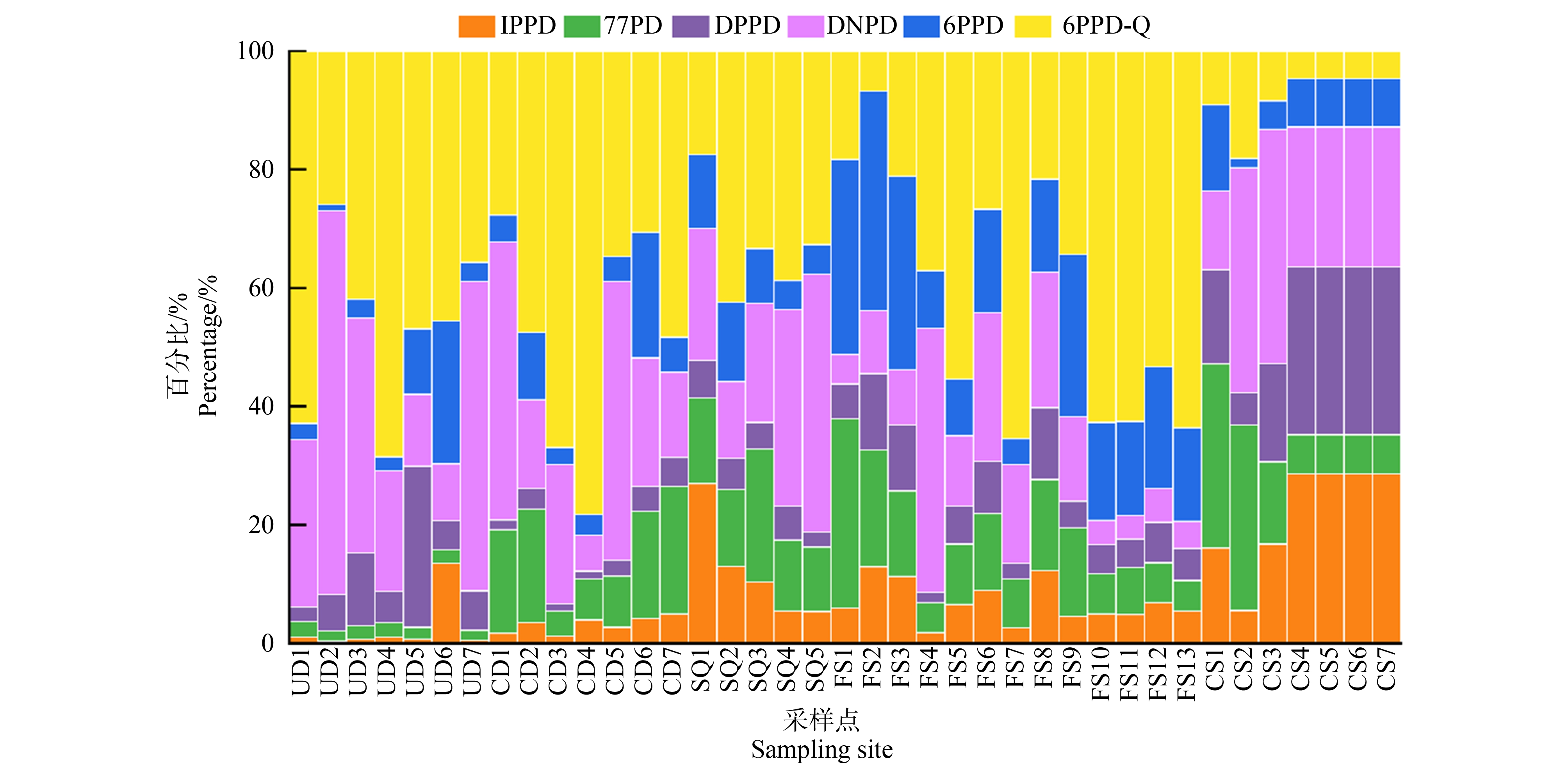
图3 道路尘土和附近表层土中目标化合物的组成
Fig. 3 Composition of target compounds in road dust and nearby topsoil

图4 PPDs和6PPD-Q的浓度相关性
注:(a) 5种PPDs和6PPD-Q的Pearson相关性;(b) 6PPD和6PPD-Q的相关性拟合。
Fig. 4 Correlation between the concentration of PPD and 6PPD-Q in the sample
Note: (a) Pearson’s rank correlation for PPDs and 6PPD-Q; (b) Correlation between 6PPD and 6PPD-Q concentrations.
2.3 PPDs与6PPD-Q浓度相关性分析
采用Pearson相关分析法检验了不同区域尘土样品及表层土样品中ΣPPDs和6PPD-Q浓度之间的相关性。除77PD外,所有PPDs和6PPD-Q的浓度均呈显著正相关。常用抗氧化剂6PPD浓度与DPPD(ρ = 0.80)和DNPD(ρ = 0.83)的浓度呈强相关(P ≤ 0.001),表明三者具有相似的来源。6PPD是商用轮胎配方中添加量最大的一种对苯二胺类抗氧化剂,添加量约为1%~4%[33-35],另外DPPD和DNPD也是常用的抗氧化剂[36]。本研究的39个道路尘土以及土壤样品中,6PPD与6PPD-Q的浓度之间存在着强烈的线性相关(r = 0.78,P <0.01),由于6PPD-Q是6PPD与臭氧反应的产物,其高相关性表明6PPD-Q的累积对6PPD在尘土中的环境存量有明显的依赖性。
2.4 ΣPPDs和6PPD-Q的人体暴露评估
道路尘土中PPDs及氧化产物6PPD-Q可能经口和皮肤进入人体,根据本研究在不同环境尘土中测得的目标化合物浓度,我们估算了该类污染物的成人和儿童的每日摄入量,以初步评估其人体健康风险。在此评估中,经口摄入和皮肤吸收被认为是平行进行的。儿童与成人通过尘土经皮肤吸收和经口摄入的5种PPDs以及6PPD-Q每日摄入量如图5所示。

图5 儿童和成人ΣPPDs和6PPD-Q日摄入量分析
注:DI表示目标化合物的日摄入量,DIing表示经口摄入量,DIder表示经皮肤摄入量
Fig. 5 Daily intakes of ΣPPDs and 6PPD-Q in children and adults
Note: DI indicates daily intake of the target compound, DIing indicates oral intake and DIder indicates dermal intake.
结果表明,无论成人还是儿童,ΣPPDs和6PPD-Q的经口摄入量均大于皮肤吸收量,对于儿童而言,ΣPPDs和6PPD-Q经口摄入量分别为0.10 ng·kg-1·d-1和0.08 ng·kg-1·d-1;对于成人而言,ΣPPDs和6PPD-Q经口摄入量分别为0.06 ng·kg-1·d-1和0.04 ng·kg-1·d-1。ΣPPDs和6PPD-Q在3种不同尘土环境中的摄入量呈现相同的趋势,均为主干道尘土>>居民区道路尘土>居民广场道路尘土,3种尘土样品中ΣPPDs的日摄入量分别为0.12、0.03、0.02 ng·kg-1·d-1,6PPD-Q的日摄入量分别为0.09、0.04、0.01 ng·kg-1·d-1。儿童与成人的日摄入量存在差异,儿童对于ΣPPDs的总摄入量为0.12 ng·kg-1·d-1,成人摄入量仅为儿童的近50%;对于6PPD-Q,儿童的摄入量为0.09 ng·kg-1·d-1,而成人仅为0.05 ng·kg-1·d-1,表明该类化合物的儿童暴露量显著高于成人。
3 讨论(Discussion)
本研究对与居民生活密切相关的不同环境中尘土以及表层土中的PPDs和6PPD-Q进行了污染特征分析和暴露评估,阐明了不同环境中PPDs和6PPD-Q的复合污染概况,将不同区域尘土以及表层土样品中的PPDs和6PPD-Q的存在水平进行对比,并进一步分析其不同的污染特征。结果表明,6PPD、6PPD-Q、DNPD和77PD在道路尘土样品中的检出率均为100%;农田表层土样品中77PD、6PPD和6PPD-Q的检出率均为100%;在居民区绿化带表层土中6种目标物质的检出率均低于50%,CPPD在所有样品中均未检到。6PPD-Q浓度最高,和ΣPPDs具有相同的浓度分布趋势,即主干道尘土>居民区道路尘土>居民广场尘土>农田表层土>绿化带表层土,ΣPPDs和6PPD-Q在道路尘土中的含量远高于表层土。将主干道尘土作为ΣPPDs和6PPD-Q的主要来源介质,我们可以看出,ΣPPDs和6PPD-Q能够随着“主干道尘土-居民区道路尘土-居民广场尘土-绿化带表层土”的路径迁移而浓度水平和检出率逐渐降低。本研究不同环境尘土中PPDs组成存在较大差异,车流量较大的城市主干道中,DPPD、DNPD、6PPD含量最高,这可能由于这3种物质被广泛用于商用车轮胎配方中[32-33]。另外,除了主干道尘土,居民区道路尘土中77PD检出率也为100%,这可能由于77PD可用于居民区内电线的橡胶涂层[37]。农田表层土中的77PD、6PPD和6PPD-Q含量及检出率均高于绿化带表层土。本研究绿化带表层土均选自无汽车通行居民小区,目标化合物浓度偏低且检出率均低于50%,而农田表层土均采集自高速公路两侧10 m内的农田。不同环境之间的浓度的差异表明,汽车通行乃至橡胶轮胎的使用对PPDs和6PPD-Q污染情况有很大影响,轮胎在道路上摩擦形成的磨损颗粒可能是这些橡胶添加剂释放的主要途径[38]。此外,PPDs还可能被应用于染发剂[9]、指甲油染料[10]、润滑剂[11]等的制备,这些均与居民生活息息相关,所以,居民区道路尘土、居民广场尘土以及居民区绿化带表层土中的PPDs可能并不仅来源于橡胶轮胎磨损,而是多种因素综合作用。
本研究中主干道尘土中ΣPPDs浓度水平(中值:62.64 ng·g-1)低于日本东京主干道(中值:329 ng·g-1)[28]和中国广州市道路尘土(中值:156 ng·g-1)[8],高于中国南方某电子垃圾拆解区周边家庭客厅尘土(中值:14 ng·g-1)[8]。本研究中主干道尘土中6PPD-Q的检出水平(中值:42.33 ng·g-1)远低于日本东京主干道(中值:809 ng·g-1)[28]、中国香港新界和九龙地区交通密集道路(中值:234 ng·g-1)[27]和广州市主干道(中值:122 ng·g-1)[8]。推测单位时间内车流量可能是引起PPDs和6PPD-Q浓度差异的主要原因。健康风险评估表明,经口摄入是人体接触PPDs和6PPD-Q的主要途径。儿童与成年人经皮肤吸收占经口摄入量的14.95%~19.52%。儿童6PPD-Q的总摄入量估计为0.09 ng·kg-1·d-1,低于其母体化合物的剂量(0.12 ng·kg-1·d-1);成人6PPD-Q的总摄入量估计为0.05 ng·kg-1·d-1,略低于其母体化合物的剂量(0.07 ng·kg-1·d-1)。儿童暴露于尘土中ΣPPDs及6PPD-Q的健康风险大于成人的主要原因是:儿童单位体质量的摄入比成人多,且具有相对频繁的手对口的行为。鉴于对苯二胺类抗氧化剂的广泛使用以及橡胶轮胎磨损颗粒的持续产生,道路尘土中6PPD-Q的高水平存在对成年人及儿童具有潜在的健康风险。成人对于3种尘土样品中6PPD的日摄入量分别为0.005、0.001、0.001 ng·kg-1·d-1,儿童对于3种尘土样品中6PPD的日摄入量分别为0.005、0.002、0.002 ng·kg-1·d-1。Liu等[39]的研究中,儿童对于室内尘土、操场尘土中6PPD的每日摄入量中值分别为0.04 ng·kg-1·d-1和0.11 ng·kg-1·d-1,成人对于室内尘土中6PPD的日摄入量中值为0.008 ng·kg-1·d-1。本研究所得6PPD日摄入量远低于Liu等的研究。就6PPD-Q而言,作为新出现的污染物,我们无法获得它的允许日摄入量值。然而,尘土中6PPD-Q的日摄入量与尘土中全氟和多氟烷基物质(PFAS)[40]处于同一水平,但低于有机磷酸酯(OPEs)[41]的日摄入量。
[1] Huntink N M, Datta R N, Noordermeer J W M. Addressing durability of rubber compounds [J]. Rubber Chemistry and Technology, 2004, 77(3): 476-511
[2] Tian Z Y, Zhao H Q, Peter K T, et al. A ubiquitous tire rubber-derived chemical induces acute mortality in coho salmon [J]. Science, 2021, 371(6525): 185-189
[3] 吕咏梅. 对苯二胺类橡胶防老剂技术进展及市场需求分析[J]. 橡胶科技市场, 2010, 8(21): 1-5
[4] Datta R N, Huntink N M, Datta S, et al. Rubber vulcanizates degradation and stabilization [J]. Rubber Chemistry and Technology, 2007, 80(3): 436-480
[5] Klauschies T, Isanta-Navarro J. The joint effects of salt and 6PPD contamination on a freshwater herbivore [J]. Science of the Total Environment, 2022, 829: 154675
[6] 朱勇, 丁璐, 徐艳琼. 橡胶防老剂4020、4010NA对人胚肺成纤维细胞的毒性对比[J]. 职业与健康, 2016, 32(14): 1991-1992, 1996
Zhu Y, Ding L, Xu Y Q. A comparative study of toxicity of rubber antioxidant 4020 and 4010NA on human embryonic lung fibroblast cells [J]. Occupation and Health, 2016, 32(14): 1991-1992, 1996 (in Chinese)
[7] Matsumoto M, Yamaguchi M, Yoshida Y, et al. An antioxidant, N,N’-diphenyl-p-phenylenediamine (DPPD), affects labor and delivery in rats: A 28-day repeated dose test and reproduction/developmental toxicity test [J]. Food and Chemical Toxicology: An International Journal Published for the British Industrial Biological Research Association, 2013, 56: 290-296
[8] Huang W, Shi Y M, Huang J L, et al. Occurrence of substituted p-phenylenediamine antioxidants in dusts [J]. Environmental Science &Technology Letters, 2021, 8(5): 381-385
[9] 李嘉瑶, 申慧敏, 徐婷婷, 等. 橡胶防老化剂6PPD及其臭氧化产物6PPD-Q的环境分布和生物毒性[J]. 中国环境科学, 2023, 43(3): 1407-1421
Li J Y, Shen H M, Xu T T, et al. Rubber anti-aging agent 6PPD and its ozonation product 6-PPDQ: Environmental distribution and biological toxicity [J]. China Environmental Science, 2023, 43(3): 1407-1421 (in Chinese)
[10] Meyer A, Fischer K. Oxidative transformation processes and products of para-phenylenediamine (PPD) and para-toluenediamine (PTD)—A review [J]. Environmental Sciences Europe, 2015, 27(1): 11
[11] Hartwig A. N-(1,3-dimethylbutyl)-N’-phenyl-p-phenylenediamine (6-PPD) [MAK Value Documentation, 2013] [J]. The MAK-Collection for Occupational Health and Safety: Annual Thresholds and Classifications for the Workplace, 2002, 1(2): 746-770
[12] Deng C L, Huang J L, Qi Y Q, et al. Distribution patterns of rubber tire-related chemicals with particle size in road and indoor parking lot dust [J]. The Science of the Total Environment, 2022, 844: 157144
[13] Liang B W, Li J H, Du B B, et al. E-waste recycling emits large quantities of emerging aromatic amines and organophosphites: A poorly recognized source for another two classes of synthetic antioxidants [J]. Environmental Science &Technology Letters, 2022, 9(7): 625-631
[14] Wu Y, Venier M, Hites R A. Broad exposure of the North American environment to phenolic and amino antioxidants and to ultraviolet filters [J]. Environmental Science &Technology, 2020, 54(15): 9345-9355
[15] Zhang Y J, Xu T T, Ye D M, et al. Widespread N-(1,3-dimethylbutyl)-N’-phenyl-p-phenylenediamine quinone in size-fractioned atmospheric particles and dust of different indoor environments [J]. Environmental Science &Technology Letters, 2022, 9(5): 420-425
[16] Klöckner P, Seiwert B, Weyrauch S, et al. Comprehensive characterization of tire and road wear particles in highway tunnel road dust by use of size and density fractionation [J]. Chemosphere, 2021, 279: 130530
[17] Wang W, Cao G D, Zhang J, et al. p-phenylenediamine-derived quinones as new contributors to the oxidative potential of fine particulate matter [J]. Environmental Science &Technology Letters, 2022, 9(9): 712-717
[18] Wang W, Cao G D, Zhang J, et al. Beyond substituted p-phenylenediamine antioxidants: Prevalence of their quinone derivatives in PM2.5 [J]. Environmental Science &Technology, 2022, 56(15): 10629-10637
[19] Challis J K, Popick H, Prajapati S, et al. Occurrences of tire rubber-derived contaminants in cold-climate urban runoff [J]. Environmental Science &Technology Letters, 2021, 8(11): 961-967
[20] Johannessen C, Helm P, Lashuk B, et al. The tire wear compounds 6PPD-quinone and 1,3-diphenylguanidine in an urban watershed [J]. Archives of Environmental Contamination and Toxicology, 2022, 82(2): 171-179
[21] Monaghan J, Jaeger A, Agua A R, et al. A direct mass spectrometry method for the rapid analysis of ubiquitous tire-derived toxin N-(1,3-dimethylbutyl)-N’-phenyl-p-phenylenediamine quinone (6-PPDQ) [J]. Environmental Science &Technology Letters, 2021, 8(12): 1051-1056
[22] Peng Z F, Zhang W F, Yin D, et al. Novel magnetic single-layer nano-MXene as a highly effective adsorbent and new SALDI-TOF-MS matrix for enrichment and rapid determination of p-phenylenediamine antioxidants in water [J]. Chemical Engineering Journal, 2023, 454: 139978
[23] Klöckner P, Seiwert B, Wagner S, et al. Organic markers of tire and road wear particles in sediments and soils: Transformation products of major antiozonants as promising candidates [J]. Environmental Science &Technology, 2021, 55(17): 11723-11732
[24] Zhang Z F, Zhang X E, Sverko E, et al. Determination of diphenylamine antioxidants in wastewater/biosolids and sediment [J]. Environmental Science &Technology Letters, 2020, 7(2): 102-110
[25] Ji J W, Li C S, Zhang B J, et al. Exploration of emerging environmental pollutants 6PPD and 6PPDQ in honey and fish samples [J]. Food Chemistry, 2022, 396: 133640
[26] Du B B, Liang B W, Li Y, et al. First report on the occurrence of N-(1,3-dimethylbutyl)-N’-phenyl-p-phenylenediamine (6PPD) and 6PPD-quinone as pervasive pollutants in human urine from South China [J]. Environmental Science &Technology Letters, 2022, 9(12): 1056-1062
[27] Cao G D, Wang W, Zhang J, et al. New evidence of rubber-derived quinones in water, air, and soil [J]. Environmental Science &Technology, 2022, 56(7): 4142-4150
[28] Hiki K, Yamamoto H. Concentration and leachability of N-(1,3-dimethylbutyl)-N’-phenyl-p-phenylenediamine (6PPD) and its quinone transformation product (6PPD-Q) in road dust collected in Tokyo, Japan [J]. Environmental Pollution, 2022, 302: 119082
[29] Wu Y, Moore J, Guo J H, et al. Multi-residue determination of polyhalogenated carbazoles in aquatic sediments [J]. Journal of Chromatography A, 2016, 1434: 111-118
[30] Ji Y Q, Wang F M, Zhang L B, et al. A comprehensive assessment of human exposure to phthalates from environmental media and food in Tianjin, China [J]. Journal of Hazardous Materials, 2014, 279: 133-140
[31] Zhang J, Zhang X F, Wu L, et al. Occurrence of benzothiazole and its derivates in tire wear, road dust, and roadside soil [J]. Chemosphere, 2018, 201: 310-317
[32] Fohet L, Andanson J M, Charbouillot T, et al. Time-concentration profiles of tire particle additives and transformation products under natural and artificial aging [J]. The Science of the Total Environment, 2023, 859(Pt 1): 160150
[33] Cataldo F, Ursini O, Angelini G. Biodiesel as a plasticizer of a SBR-based tire tread formulation [J]. ISRN Polymer Science, 2013, 2013: 1-9
[34] Hough P, van der Aar N, Qiu Z Y. Compounding and mixing methodology for good performance of EPDM in tire sidewalls [J]. Tire Science and Technology, 2020, 48(1): 2-21
[35] Waddell W H, Evans L R. Use of nonblack fillers in tire compounds [J]. Rubber Chemistry and Technology, 1996, 69(3): 377-423
[36] Cataldo F. Early stages of p-phenylenediamine antiozonants reaction with ozone: Radical cation and nitroxyl radical formation [J]. Polymer Degradation and Stability, 2018, 147: 132-141
[37] European Commission. Information from the REACH registration dossiers of 77PD [DB/OL]. (2023-03-02) [2023-03-19]. https://echa.europa.eu/information-on-chemicals.
[38] Wagner S, Hüffer T, Klöckner P, et al. Tire wear particles in the aquatic environment - A review on generation, analysis, occurrence, fate and effects [J]. Water Research, 2018, 139: 83-100
[39] Liu R Z, Li Y L, Lin Y F, et al. Emerging aromatic secondary amine contaminants and related derivatives in various dust matrices in China [J]. Ecotoxicology and Environmental Safety, 2019, 170: 657-663
[40] 方淑红, 朱和祥, 叶芝祥, 等. 成都市道路积尘中全氟化合物的污染特征及暴露风险评估[J]. 环境科学, 2019, 40(12): 5265-5271
Fang S H, Zhu H X, Ye Z X, et al. Pollution characteristics and exposure risk assessment of perfluoroalkyl substances in road dust, Chengdu [J]. Environmental Science, 2019, 40(12): 5265-5271 (in Chinese)
[41] Li W H, Shi Y L, Gao L H, et al. Occurrence, distribution and risk of organophosphate esters in urban road dust in Beijing, China [J]. Environmental Pollution, 2018, 241: 566-575