-
随着我国生活污水中氮磷浓度不断增加,高氮磷、低碳氮(C/N)比生活污水愈发常见[1-2]。此类生活污水常因有机碳源不足而导致二级生化处理工艺对总氮(TN)和总磷(TP)的去除有限[3]。超标的氮磷排入水体将直接导致水体富营养化乃至黑臭水体的产生[2,4]。因此,开发快速高效的高氮磷、低C/N比污水处理技术对水体受纳氮磷的削减及水污染控制具有重要意义。
作为一种高级氧化技术,电化学氧化已得到高度关注[5-7]。其电解过程中产生的自由基(HO·和O2·)和阳极/阴极的氧化/还原反应而可高效去除污水中的有机物、氨氮(
$ {\rm{NH}}_4^ + $ -N)和硝酸盐氮($ {\rm{NO}}_3^ {-} $ -N)等污染物,且催化电极的使用使其氧化能力进一步提高。Ti(RuO2)电极是一种常用的电氧化电极材料,其应用显著提高了电氧化系统的氧化还原效率[7]。三维电极技术是填充床电氧化技术的统称,其填充物可为金属、金属氧化物、负载金属/金属氧化物的颗粒及具有一定吸附/沉淀能力的颗粒填料。填充物的添加可强化系统内的传质过程并提高电氧化技术的电流效率,从而在较低的能耗下取得较高的去除效果[5]。废铁屑是钢铁厂或金属加工厂产生的主要固体废物。作为水处理系统填充物,其具有价格低廉、活性高等优点[8-12]。将其合理地应用于污水处理不仅可有效提高污水处理效能、降低水处理成本,而且可以实现以废治废。已有研究已将其用于强化生物脱氮[8-10],以及以其为填充物构建三维电极来提高电氧化技术对工业废水中难降解有机物的降解效能[11-12]。但利用废铁屑强化三维电极处理高氮磷、低C/N比污水的研究仍鲜见报道。本研究将废铁屑填入电解槽,形成废铁屑-Ti(RuO2)三维电极,以实际高氮磷、低C/N比生活污水为处理对象进行实验研究。系统利用电氧化产生的自由基(HO·)的氧化能力将污水中的
$ {\rm{NH}}_4^ + $ -N氧化而去除(式(1)~式(3));$ {\rm{NO}}_3^ {-} $ -N在电阴极获得电子而被还原去除(式(4)和式(5))[5]。且废铁屑的投加不仅可提高系统的氧化能力,其原位产生的三价铁离子(Fe3+)可与磷酸盐沉淀而去除[10,13]。此外,有研究[14]表明,在有Cl−存在的情况下,电极的催化氧化作用可将Cl−氧化为氯气(Cl2)和次氯酸(HClO)等活性中间物质。根据折点加氯理论,$ {\rm{NH}}_4^ + $ -N可被氯气(Cl2)和次氯酸(HClO)直接氧化为N2。由此可见,电氧化中Cl−的投加具有降低电氧化$ {\rm{NH}}_4^ + $ -N过程中$ {\rm{NO}}_3^ {-} $ -N、亚硝氮($ {\rm{NO}}_2^ {-} $ -N)的积累,实现真正意义上的TN脱除。因此,本研究也考察了Cl−的投加对废铁屑-Ti(RuO2)三维电极脱氮的强化作用。
全文HTML
-
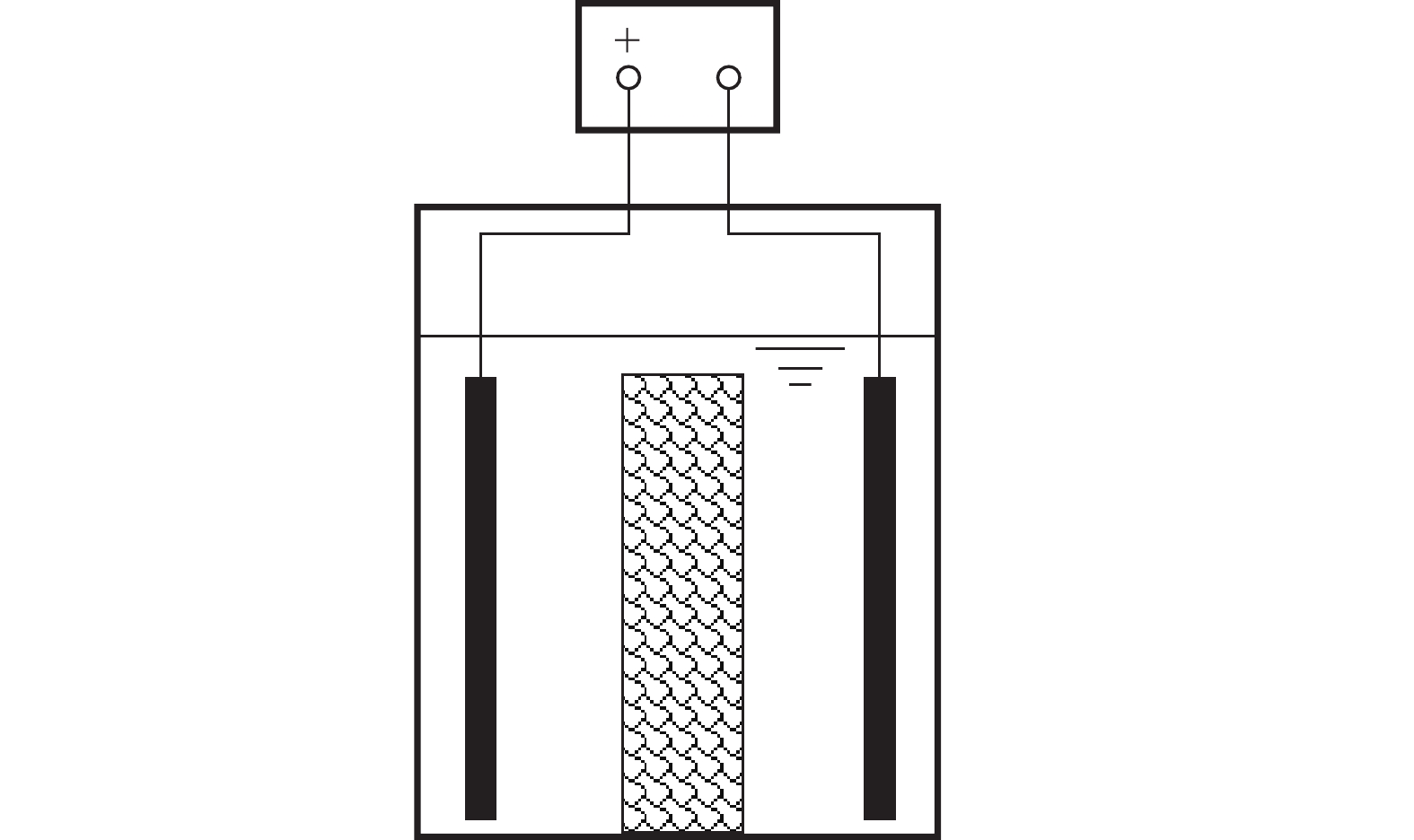
实验采用低压电场电氧化三维电极,如图1所示。装置由直流电源、聚四氟乙烯电解槽、Ti(RuO2)电极板及铁屑填充槽组成。电解槽内部尺寸为150 mm×120 mm×150 mm,有效容积为2.7 L。在序批实验中,每组实验水量为1.5 L。电极板尺寸为120 mm×80 mm×2 mm,两侧极板距电解槽壁10 mm。反应器中央设铁质网状填充槽(宽80 mm,高120 mm),用于装填废铁屑,填充槽距左右极板各25 mm,形成废铁屑-Ti(RuO2)三维电极。铁屑购自北京某钢铁厂,粒度为10~50目,零价铁(Fe0)的含量为88%~95%,其杂质主要为碳(0.5%~1%)、氧化铁(2%~4%)和四氧化三铁(3%~8%)。电源使用高频开关电源(OSIMU,江苏苏州),电源最大电压为30 V、最大电流为100 A。
-
实验挑选典型的实际高氮磷、低C/N比生活污水(取自兰州市某居民小区排水管网检查井)为研究对象,TN为131.6~145.9 mg·L−1、
$ {\rm{NH}}_4^ + $ -N为130.4~142.8 mg·L−1、$ {\rm{NO}}_3^ {-} $ -N为0.24~3.6 mg·L−1、$ {\rm{NO}}_2^ {-} $ -N为0.09~0.94 mg·L−1、TP为7.4~9.2 mg·L−1、COD为261.5~398.6 mg·L−1、pH为7.49~7.92。如表1所示,采用续批实验分别考察了以下3点:铁屑的填充(体积分数分别为0、15%、30%和45%)对Ti(RuO2)电极电氧化的强化作用;槽电压(6、8、10和12 V)和反应时间(20、40、60和80 min)的变化对Ti(RuO2)电极电氧化的影响;Cl−(NaCl)的投加量(Cl−与$ {\rm{NH}}_4^ + $ 的摩尔比R为0、2∶1、4∶1、6∶1)对$ {\rm{NH}}_4^ + $ -N直接氧化脱除的催化作用。实验均在室温(23~26 ℃)下进行。在每一取样点取3个平行样进行检测,并求得平均值和标准偏差。研究中采用拟一级反应动力学模型(式(1))对$ {\rm{NH}}_4^ + $ -N、TN和TP的去除进行动力学分析[5,12]。式中:k为反应速率常数,min−1;t为反应时间,min;Ct为时间t时污染物浓度,mg·L−1;C0为污染物初始浓度,mg·L−1。
-
本研究中,水质分析参考文献中的方法[15],对水中的
$ {\rm{NH}}_4^ + $ -N、$ {\rm{NO}}_3^ {-} $ -N、$ {\rm{NO}}_2^ {-} $ -N、TP、COD、Fe2+和总铁(TFe)浓度进行检测。其中,$ {\rm{NH}}_4^ + $ -N采用纳氏试剂分光光度法测定,$ {\rm{NO}}_3^ {-} $ -N采用紫外分光光度法测定,$ {\rm{NO}}_2^ {-} $ -N采用N-(1-萘基)-乙二胺光度法测定,TP采用钼锑抗分光光度法测定,COD采用重铬酸钾法测定,Fe2+浓度采用邻菲啰啉分光光度法测定,TFe浓度采用盐酸羟胺还原-邻菲啰啉分光光度法测定。TN浓度为$ {\rm{NH}}_4^ + $ -N、$ {\rm{NO}}_3^ {-} $ -N、$ {\rm{NO}}_2^ {-} $ -N浓度之和[16]。Fe3+浓度为TFe和Fe2+浓度之差。以上检测均利用紫外-可见分光光度计(UV5,梅特勒-托利多,上海)完成,分析过程用水均为去离子水。
1.1. 实验装置
1.2. 实验污水及实验设计
1.3. 水质分析方法
-
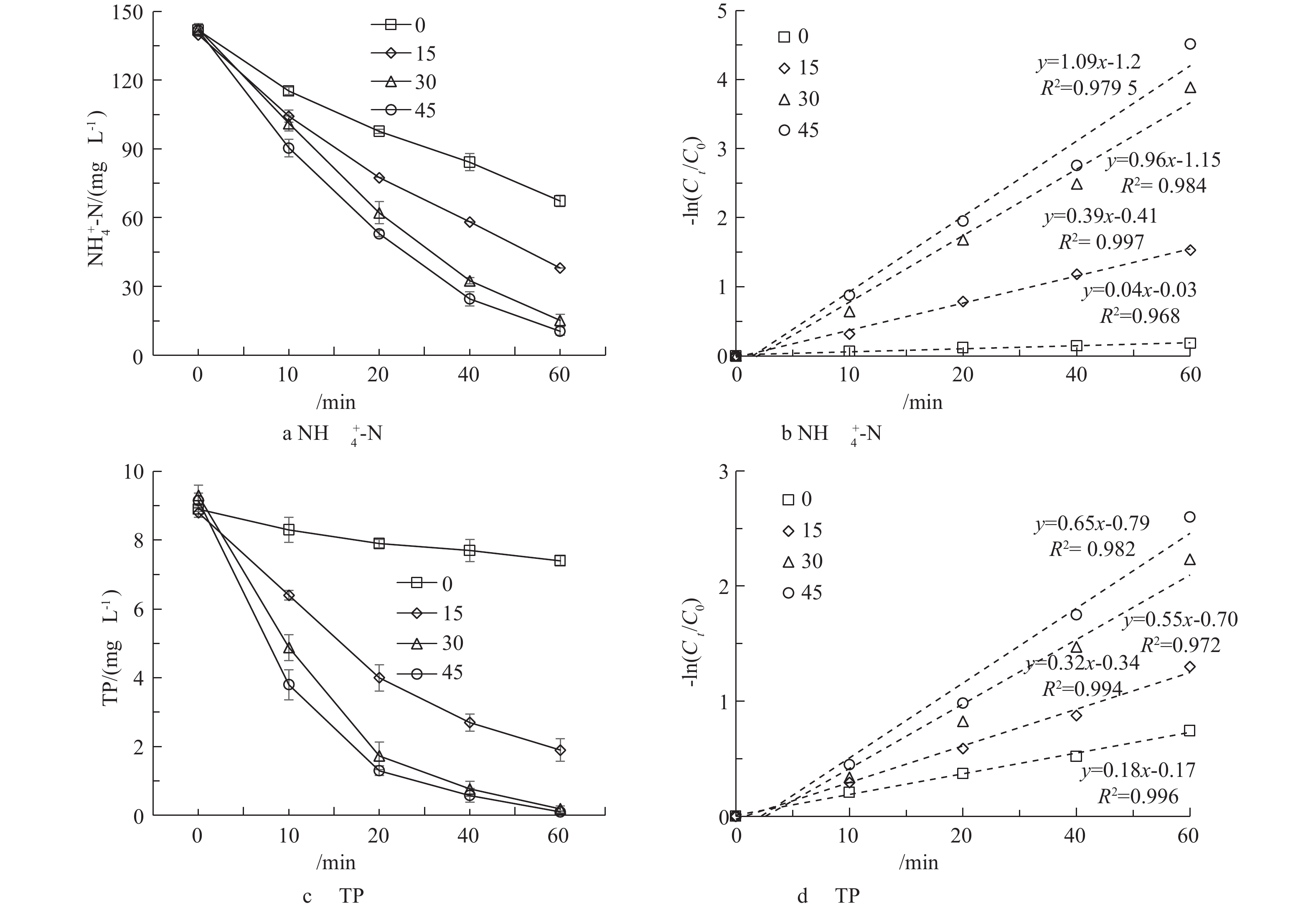
利用废铁屑构建废铁屑-Ti(RuO2)三维电极氧化体系,将槽电压稳定在12 V。在不同铁屑填充比下,考察在反应时间60 min 内COD、
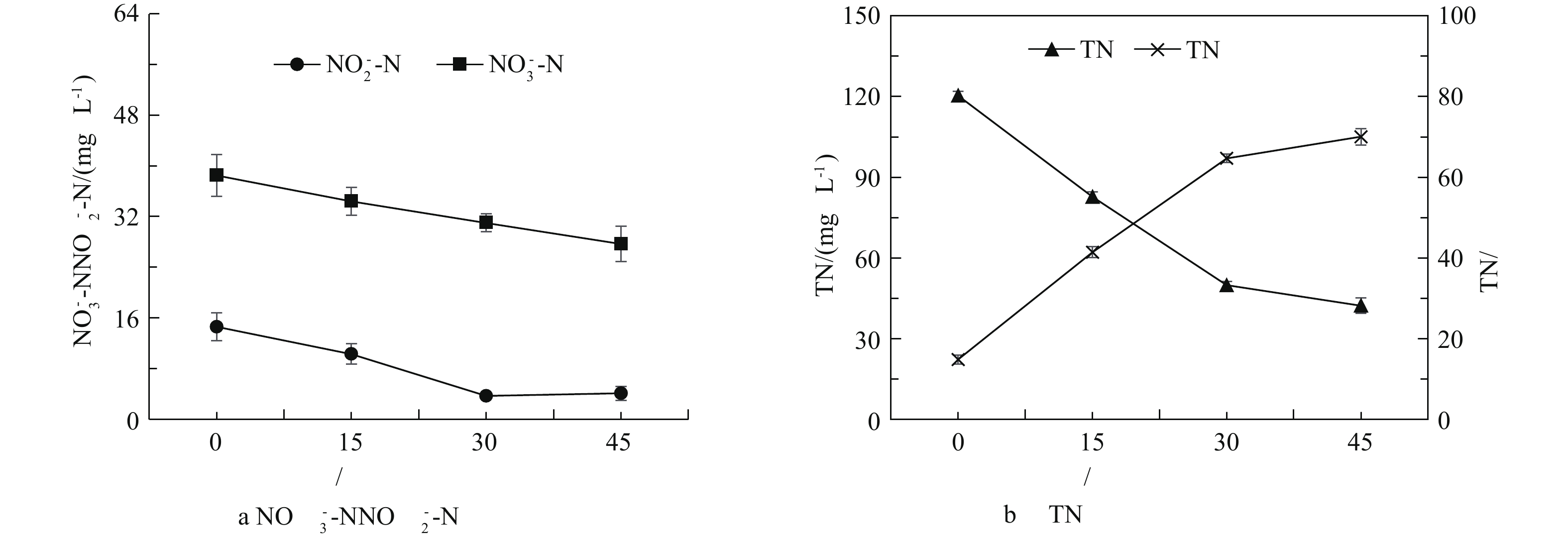
$ {\rm{NH}}_4^ + $ -N、$ {\rm{NO}}_3^ {-} $ -N、$ {\rm{NO}}_2^ {-} $ -N和TP浓度的变化情况,并对其进行动力学分析。$ {\rm{NH}}_4^ + $ -N和TP浓度的变化情况及动力学分析结果如图2所示,$ {\rm{NO}}_3^ {-} $ -N、$ {\rm{NO}}_2^ {-} $ -N和TN的变化见图3。结果表明,当槽电压为12 V、填充量(占总反应体积的体积分数)分别为0、15%、30%和45%时,电解过程电流分别为87~95、123~168、220~239和317~350 mA。当铁投加量为0、15%、30%和45%时,COD的去除率分别为71.6%、86.7%、93.5%和94.3%,在铁投加量升高至30%时,COD去除率提高了19.9%。由图2(a)可知,废铁屑的投加可有效强化电氧化对$ {\rm{NH}}_4^ + $ -N的氧化效能,当铁投加量分别为0、15%和30%、反应60 min时的$ {\rm{NH}}_4^ + $ -N去除率分别为57.5%、72.7%和89.3%。而当铁屑投加量继续提高至45%时,$ {\rm{NH}}_4^ + $ -N去除率仅升高至92.6%,这表明继续提高铁屑投加量对去除率的影响不明显。因此,确定废铁屑-Ti(RuO2)三维电极最佳铁屑填充率为30%。由图2(b)中拟一级反应动力学的拟合方程可知,此时$ {\rm{NH}}_4^ + $ -N降解反应速率常数由0.18 min−1显著提高至0.55 min−1。这表明废铁屑的投加显著提高了电氧化系统的电流效率,从而提高了$ {\rm{NH}}_4^ + $ -N的氧化速率。由图2(c)显示,废铁屑的投加显著提高了电氧化系统的除磷效率。当投加率为30%、反应60 min时的TP去除率由未投加铁时的16.9%提升至96.7%,出水TP浓度降至0.31 mg·L−1。此时,TN降解反应速率常数由0.04 min−1显著提高至0.85 min−1。其原因为,在电氧化过程中,所填充的铁屑在电压作用下所形成微电极而发生氧化还原反应(式(6)),其阴极释放电子(e−),阳极发生铁氧化反应,生成Fe3+,$ {\rm{PO}}_4^ {3-} $ 与Fe3+生成沉淀而被去除[11-12](式(7))。经测定,当铁屑填充率为30%、反应60 min时,出水Fe2+和Fe3+的浓度分别由未投加铁屑时的0.13 mg·L−1和0.27 mg·L−1升高至8.5 mg·L−1和5.8 mg·L−1。如图3所示,投加废铁屑所形成的三维电极在一定程度上降低了电氧化系统内
$ {\rm{NO}}_3^ {-} $ -N和$ {\rm{NO}}_2^ {-} $ -N的积累,从而提高了TN的去除率。当铁投加率为30%时,TN去除率由未投加铁时的23.4%提升至64.7%,增加了41.3%。其原因为,废铁屑所形成微电极的阴极提供了更多的阴极还原位点[5],从而增强了系统对$ {\rm{NO}}_3^ {-} $ -N和$ {\rm{NO}}_2^ {-} $ -N的还原效能,进而提高了TN的去除率。故废铁屑的投加可同时强化电氧化体系对COD、$ {\rm{NH}}_4^ + $ -N、$ {\rm{NO}}_3^ {-} $ -N、$ {\rm{NO}}_2^ {-} $ -N和TP的去除,并确定其最佳投加率为30%。 -
由于电氧化需在外加电场的作用下进行,其运行能耗为其在实际应用中的主要成本[5]。而能耗主要由污水在系统内所需的反应时间及运行过程所施加的槽电压决定[5-6]。因此,本研究察了反应时间和槽电压对废铁屑-Ti(RuO2)三维电极处理效能的影响。
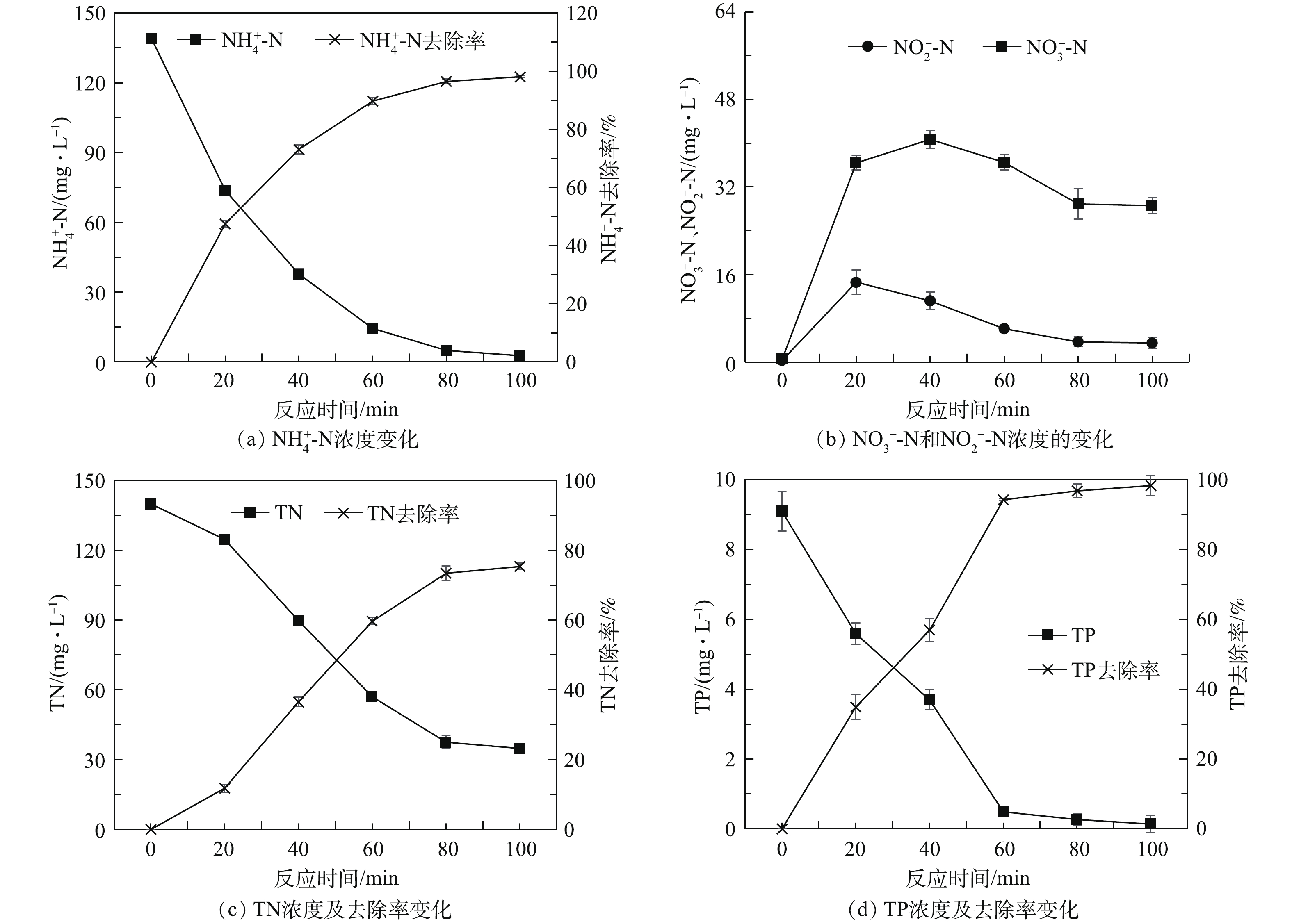
1)反应时间对系统处理效能的影响。控制铁屑投加率为30%、槽电压为12 V,考察在反应时间为20、40、60、80和100 min时废铁屑-Ti(RuO2)三维电极对污染物的去除情况,结果如图4所示。当反应时间为20、40、60、80和100 min 时,COD的去除率分别为45.2%、77.8%、93.5%、95.1%和96.4%,在60~100 min时,COD去除率提高不明显。由图4可知,
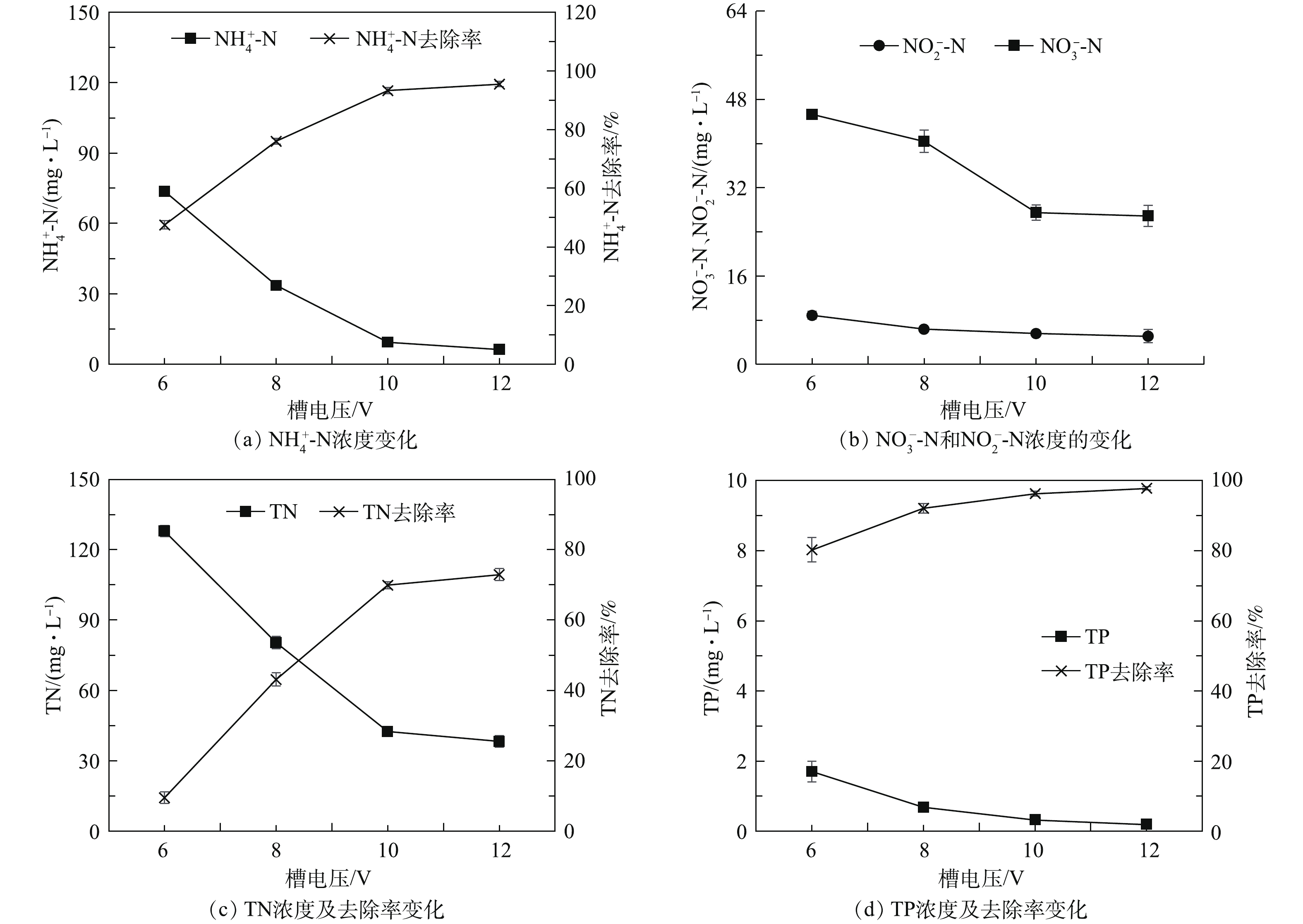
$ {\rm{NH}}_4^ + $ -N、TN和TP浓度均随着反应时间的延长而降低,表明适当延长反应时间可提高氮磷的去除。其中$ {\rm{NH}}_4^ + $ -N和TP浓度在60 min内迅速降低,去除率分别达89.6%和94.6%;在反应时间60~100 min内,$ {\rm{NH}}_4^ + $ -N和TP浓度逐渐趋于平衡。然而,$ {\rm{NO}}_3^ {-} $ -N和$ {\rm{NO}}_2^ {-} $ -N的浓度均出现先升高后降低的变化趋势,并在60~80 min继续降低,在80~100 min趋于平衡,如图3(b)所示。该变化趋势与TN在60~80 min时的持续降低相符,如图3(c)所示。当反应时间为80 min时,TN去除率达到73.5%。因此,确定废铁屑-Ti(RuO2)三维电极最佳反应时间为80 min。2)槽电压对系统处理效能的影响。控制铁屑投加率为30%、反应时间为80 min,考察在槽电压为6、8、10和12 V时废铁屑-Ti(RuO2)三维电极对污染物的去除情况如图5所示。当槽电压为6、8、10和12 V时,电解过程电流分别为97~128、149~164、189~201和220~239 mA。当槽电压为6、8、10和12 V 时,COD的去除率分别为57.2%、89.5%、92.6%和95.1%,在槽电压为6~8 V时迅速升高,在8~12 V时趋于稳定。同时,由图5可见,随着槽电压的升高,
$ {\rm{NH}}_4^ + $ -N、$ {\rm{NO}}_3^ {-} $ -N、$ {\rm{NO}}_2^ {-} $ -N、TN和TP浓度均随反应时间的延长而降低。其原因为,槽电压的升高增强了电极的氧化还原速率,使阳极HO·的产生速率及阴极的还原速率提高[17-19]。同时,槽电压的升高促进了铁屑微电极的电子和Fe3+的释放速率,从而促进了$ {\rm{NO}}_3^ {-} $ -N、$ {\rm{NO}}_2^ {-} $ -N的还原及$ {\rm{PO}}_4^ {-} $ 的固定。值得注意的是,当槽电压由6 V升高至10 V时,$ {\rm{NH}}_4^ + $ -N、TN和TP浓度迅速降低,$ {\rm{NO}}_3^ {-} $ -N和$ {\rm{NO}}_2^ {-} $ -N的积累也逐渐减小;当槽电压为10 V时,$ {\rm{NH}}_4^ + $ -N、TN和TP去除率分别达93.3%、69.9%和96.3%;而当继续将槽电压升高至12 V时,$ {\rm{NH}}_4^ + $ -N、TN和TP浓度趋于平衡,去除率分别为95.5%、72.9%和97.8%。因此,综合考虑废铁屑-Ti(RuO2)三维电极的处理效能和运行能耗,将该系统槽电压控制为10 V为宜。综上所述,本研究获得废铁屑-Ti(RuO2)三维电极最佳反应时间和槽电压分别为80 min和10 V。在本研究的低C/N比污水处理中,通过向三维电极中投加铁屑(30%),TP和COD在较低的反应时间和槽电压下即可达到较高的去除率。相比之下,TN的去除需要更长的反应时间和更高的槽电压,故TN浓度决定了最佳运行参数的选择。其原因可能在于:本研究所使用的污水TN浓度较高,而TP和COD值相对较低。故在利用该系统处理TP和COD值较高的污水时须通过实验对运行参数进行进一步优化。
-
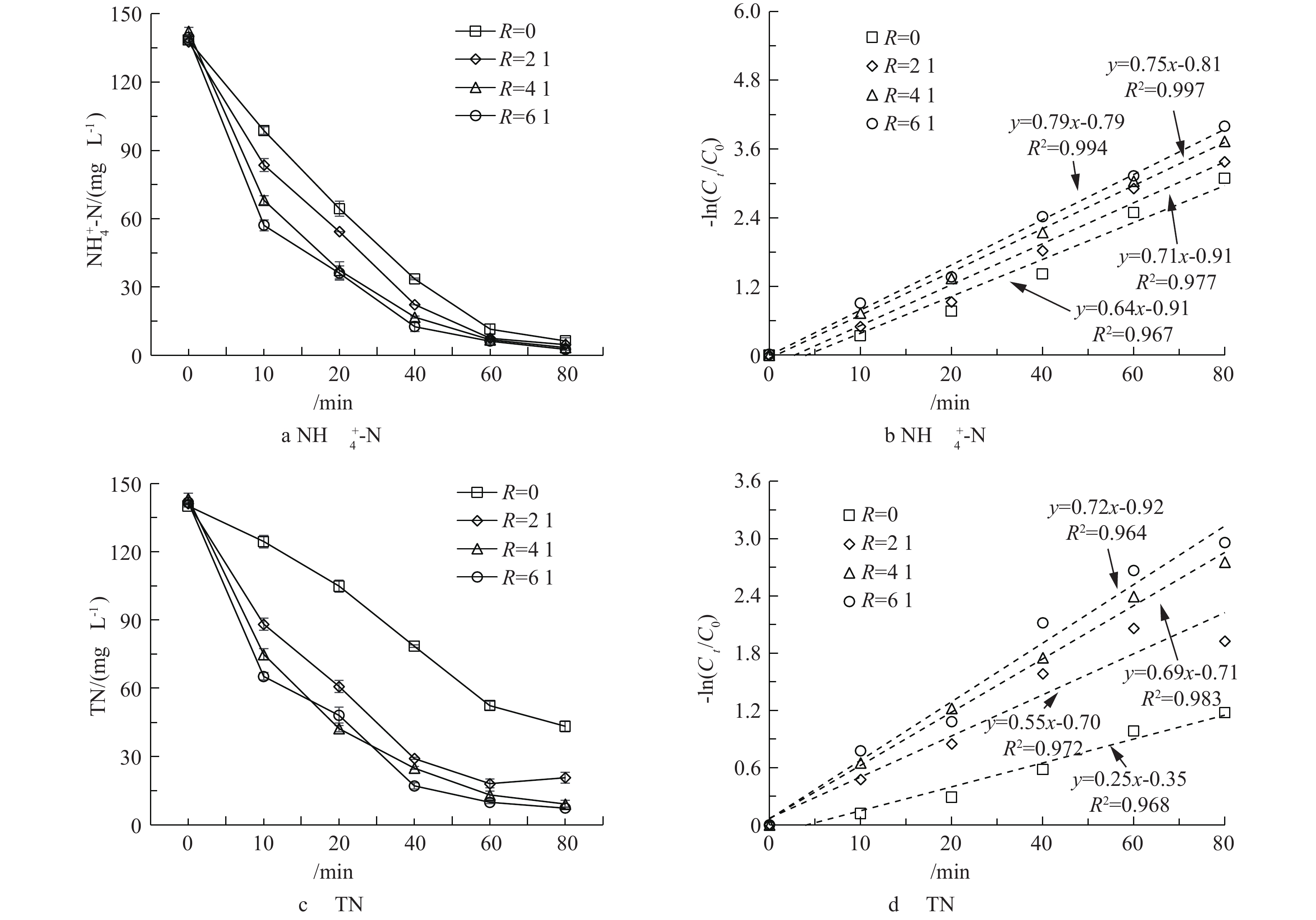
在铁屑填充率为30%时,分别控制反应时间及槽电压为80 min和10 V,探究Cl−的投加量(Cl−与
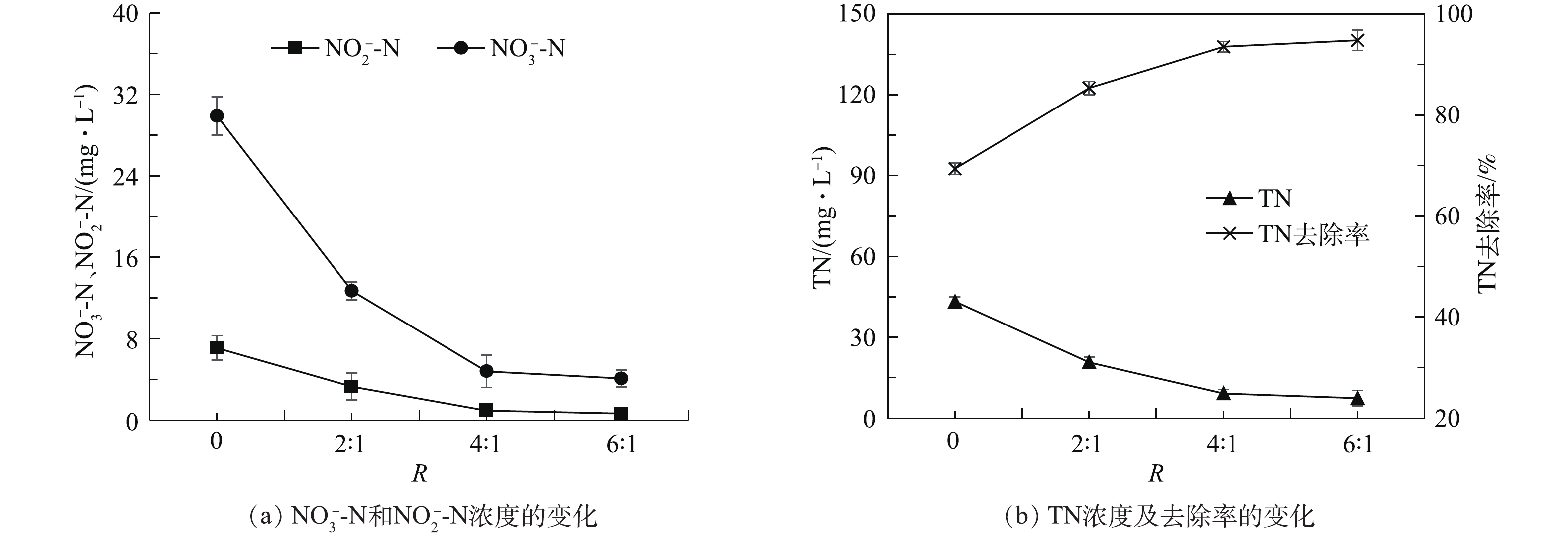
$ {\rm{NH}}_4^ + $ -N的摩尔比R)对废铁屑-Ti(RuO2)三维电极脱氮的催化作用,结果如图6和图7所示。由图6(a)可知,Cl−的投加一定程度地提高了废铁屑-Ti(RuO2)三维电极的$ {\rm{NH}}_4^ + $ -N的氧化速率。当R为0、2、4和6时,$ {\rm{NH}}_4^ + $ -N的氧化速率常数分别为0.64、0.71、0.75和0.79 min−1(图6(b))。其原因为,NaCl的投加增加了污水的导电率,有助于提高三维电极的电极效率,从而强化其氧化效能。值得注意的是,Cl−的投加对TN去除效率的提高更为明显(图6(c)~图6(d))。当R为2和4时,TN去除速率常数由未投加时的0.27 min−1分别迅速增至0.55 min−1和 0.69 min−1。同时,由图7(a)可见,Cl−的投加显著降低了
$ {\rm{NH}}_4^ + $ -N氧化过程中$ {\rm{NO}}_3^ {-} $ -N和$ {\rm{NO}}_2^ {-} $ -N的积累。因此,TN的去除表现为$ {\rm{NH}}_4^ + $ -N的直接氧化脱除。其原因为,当投加Cl−时,Cl−可在三维电极的阳极被氧化,生成Cl2,进而转化为HClO(式(8)~式(10));HClO可将$ {\rm{NH}}_4^ + $ -N直接氧化为N2,从而实现TN的脱除(式(11));而$ {\rm{NH}}_4^ + $ -N氧化过程所产生的新生态的Cl−继续参与反应,从而对$ {\rm{NH}}_4^ + $ -N的氧化起到催化作用[13-14,19]。同时,系统中仍有部分$ {\rm{NO}}_3^ {-} $ -N(4.8 mg·L−1)和$ {\rm{NO}}_2^ {-} $ -N(0.83 mg·L−1)的积累,表明$ {\rm{NH}}_4^ + $ -N的电极直接氧化作用仍在进行,但此时其借助Cl−催化的间接氧化作用占据主导地位,提高了TN的去除率(图7(b))。由图6和图7可知,当R由4升高至6时,
$ {\rm{NH}}_4^ + $ -N和TN的去除速率的增加均明显减缓。TN的去除速率常数仅由0.69 min−1增至0.72 min−1。由此可判断,废铁屑-Ti(RuO2)三维电极的最佳Cl−与$ {\rm{NH}}_4^ + $ 摩尔比为4。此时,出水$ {\rm{NH}}_4^ + $ -N、TN、COD、TP的平均浓度分别降至3.4、9.2、21.7和0.14 mg·L−1,均满足我国《城镇污水处理厂污染物排放标准》(GB 18918-2016)中一级A标准所规定的5、15、50和0.5 mg·L−1。$ {\rm{NH}}_4^ + $ -N、TN、COD、TP的平均去除率分别为96.8%、93.4%、94.2%和98.1%。其中,$ {\rm{NH}}_4^ + $ -N、TN和TP去除率显著高于其他的电氧化脱氮除磷系统[5-6, 20-21]。铁屑的投加在显著提高了COD、TN和TP去除率的同时,也降低了所需槽电压,而Cl−的投加进一步提高了TN的去除率,缩短了反应所需的时间。槽电压的降低和反应时间的缩短均有效降低了电氧化系统的能耗。因此,本研究构建的废铁屑-Ti(RuO2)三维电极可为高氮磷、低C/N比污水的快速处理提供技术支持。
2.1. 铁屑投加量对废铁屑-Ti(RuO2)三维电极处理效能的影响
2.2. 运行条件对废铁屑-Ti(RuO2)三维电极处理效能的影响
2.3. Cl−的投加对废铁屑-Ti(RuO2)三维电极脱氮的催化作用
-
1)废铁屑的投加显著提高了三维电极的电氧化效率,且所释放的Fe3+可与
$ {\rm{PO}}_4^ {3-} $ 沉淀进而去除。在最佳铁屑投加率为30% (体积分数)时,$ {\rm{NH}}_4^ + $ -N和TP的拟一级反应去除速率常数分别由未投加铁屑时的0.18 min−1和0.04 min−1显著提高至0.55 min−1和0.96 min−1。COD、$ {\rm{NH}}_4^ + $ -N、TN和TP去除率分别较未投加铁屑时提高了19.9%、31.8%、41.3%和79.8%。2)反应时间的延长和槽电压的增加均能有效提高废铁屑-Ti(RuO2)三维电极的处理效率,综合考虑处理效率和能耗,最佳反应时间为80 min,最佳槽电压为10 V。
3) Cl−的投加促进了Cl2和HClO的生成,将
$ {\rm{NH}}_4^ + $ -N直接氧化为N2,大幅降低了$ {\rm{NO}}_3^ {-} $ -N和$ {\rm{NO}}_2^ {-} $ -N积累。在Cl−投加至Cl−与$ {\rm{NH}}_4^ + $ 的最佳摩尔比量4 时,TN去除速率常数(k)由未投加Cl−时的0.27 min−1增至0.69 min−1。4)最佳运行工况下,出水
$ {\rm{NH}}_4^ + $ -N、TN、COD、TP的平均去除率分别达到96.8%、93.4%、94.2%和98.1%,其浓度分别降至3.4、9.2、21.7和0.14 mg·L−1,满足我国《城镇污水处理厂污染物排放标准》(GB 18918-2016)中的一级A标准。



















 下载:
下载: